Пус почки что это
Лапароскопический уретерокаликоанастомоз при протяженной рецидивной стриктуре пиелоуретерального сегмента справа
Б.К. Комяков, Б.Г. Гулиев, Т.Х. Аль Аттар
ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» МЗ РФ; Санкт-Петербург, Россия
Автор для связи: Гулиев Бахман Гидаятович
Тел: +7 (921) 945-34-80; e-mail: gulievbg@mail.ru
Введение
Протяженные сужения прилоханочного отдела мочеточника встречаются после хирургических вмешательств при камнях лоханки и обструкции пиелоуретерального сегмента (ПУС), а также вследствие поствоспалительных изменений. Длинные стриктуры данного участка ставят под сомнение возможность и успех пластической операции по формированию пиелоуретероанастомоза. В этих случаях анастомоз мочеточника с нижней чашечкой может быть спасительной техникой по восстановлению проходимости верхних мочевых путей и избавления пациента от нефростомического дренажа. Впервые подобная операция была выполнена K. Neuwirt в 1932 году. С этого момента в литературе встречаются публикации о результатах единичных вмешательств, только некоторые авторы приводят данные более 10 операций по Нейверту 2. Kochakarn W. et al. [1] выполнили уретерокаликоанастомоз 15 больным, причиной протяженной стриктуры прилоханочного отдела мочеточника у 12 из них были неоднократные операции по поводу нефролитиаза, у 3 — безуспешные пластики ПУС.
До внедрения эндовидеохирургии уретерокаликоанастомоз выполнялся открытым доступом. Первый лапароскопический уретерокаликоанастомоз был выполнен Cherullo E.E. et al. в 2003 году [4]. В литературе описаны результаты единичных вмешательств по Нейверту лапароскопическим или робот-ассистированным доступами 6. Мы приводим клинический случай успешного лапароскопического уретерокаликоанастомоза у молодого пациента с рецидивной протяженной стриктурой прилоханочного отдела правого мочеточника.
Материал и методы
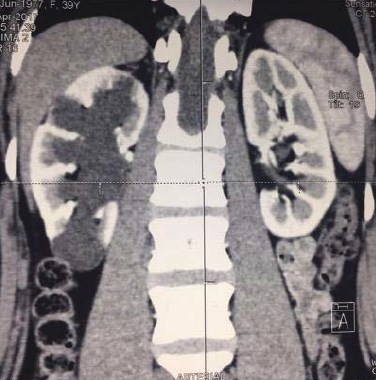
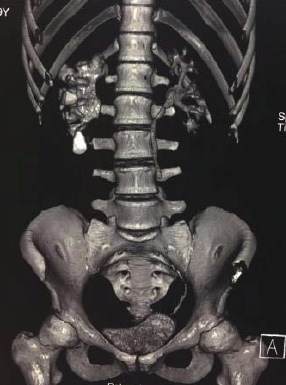
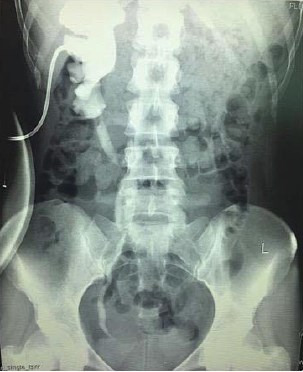
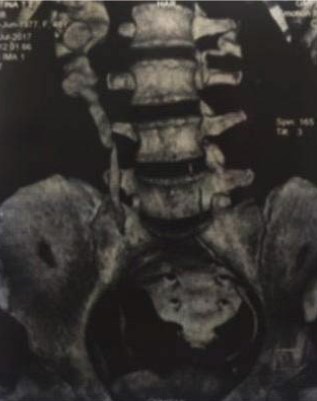
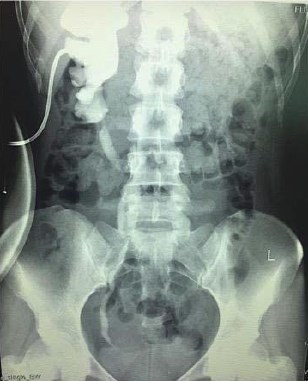
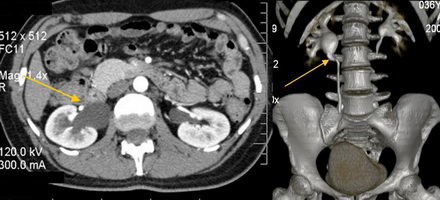
Под наблюдением находится больной 39 лет, которому 10 лет назад была выполнена открытая пиелопластика справа по Хайнс-Андерсену. После операции наблюдался только в течение первых нескольких лет. В марте 2017 года пациент обратился к урологу по месту жительства с жалобами на ноющие боли в пояснице справа. При ультразвуковом исследовании почек выявлено расширение полостной системы правой почки. Выполнена СКТ с внутривенным контрастированием и установлено, что у него имеется протяженная рецидивная стриктура прилоханочного отдела мочеточника правой почки, расширенная внутрипочечная лоханка и нижняя чашечка, истончение паренхимы над ней (рис. 1, 2). Учитывая рецидивный и протяженный характер стриктуры, сложность формирования пиелоуретероанастомоза, решено выполнить уретерокаликоанастомоз по Нейверту лапароскопическим доступом. Перед операцией под ультразвуковым контролем произведена пункционная нефростомия справа.
Рисунок 1. СКТ больного 39 лет. Полостная система правой почки расширена, паренхима над нижней чашкой истончена
Рисунок 2. КТ урография того же больного. Функция левой почки своевременная, нарушения уродинамики верхних мочевых путей слева нет. Справа расширена ЧЛС почки, ПУС не визуализируется
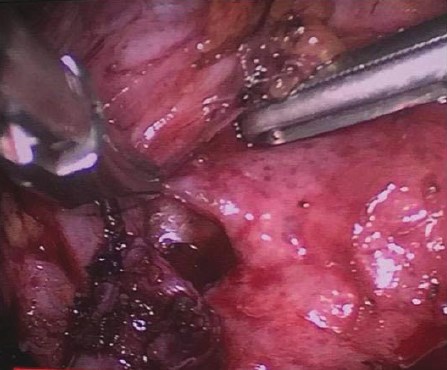
Операция выполнялась в положении на боку под общей анестезией. Первый троакар 11 мм установлен в подвздошной области, произведена диагностическая лапароскопия, далее проведены еще три троакара (один по 11 мм и два по 6 мм). Брюшина вскрыта по линии Тольда, восходящая толстая и двенадцатиперстная кишка мобилизованы и отведены медиально. Мочеточник идентифицирован на протяжении верхней трети. В области нижнего полюса и ПУС он вовлечен в выраженный рубцовый процесс, что не позволяет выделить его. Мобилизация внутрипочечной лоханки также не представляется возможной. Из-за протяженной рубцовой стриктуры ПУС решено выполнить анастомоз мочеточника с нижней чашечкой. Для этого выделен нижний полюс почки, резецирован участок истонченной паренхимы над нижней чашкой диаметром около 1,5 см (рис. 3).
Мочеточник отсечен ниже зоны стриктуры, его оставшаяся культя прошита викрилом 3/0.
Рисунок 3. Этап выполнения уретерокаликоанастомоза. Мобилизован нижний полюс почки, вскрыта нижняя чашечка
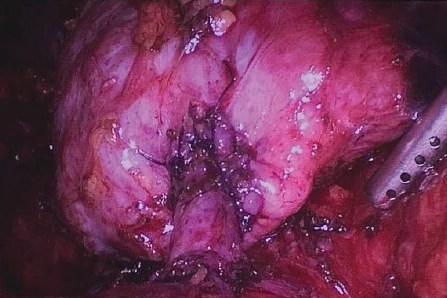
Рисунок 4. Окончательный вид уретерокаликоанастомоза
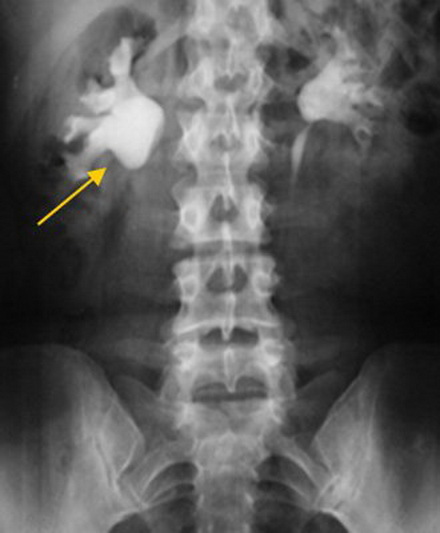
Далее произведена спатуляция мочеточника на протяжении 1,0 см. После антеградной установки стента 7 Шр, используя викрил 3/0, наложены 6 узловых швов между нижней чашкой и мочеточником (рис. 4). Герметичность анастомоза проверена введением в полостную систему почки жидкости по нефростоме. Установлен дренаж, троакары извлечены. Продолжительность составила 110 мин, кровопотеря – 50 мл. Дренаж удален на 2-е сутки, пациент выписан на амбулаторное лечение. Через 4 недели стент был извлечен, выполнена антеградная пиелография: проходимость верхних мочевых путей справа адекватная (рис. 5).
Рисунок 5. Антеградная пиелоуретерограмма через 4 недели после лапароскопического уретерокаликоанастомоза. Хорошая проходимость анастомоза и мочеточника справа
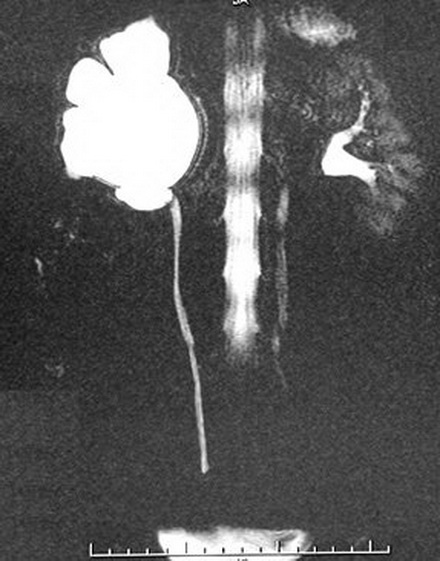
При контрольном обследовании через 6 месяцев жалоб нет, на КТ урографии функция правой почки своевременная, сохраняется расширение ЧЛС, уретерокаликоанастмоз проходим (рис. 6, 7).
Рисунок 6. КТ урограмма больного через 6 месяцев после лапароскопического уретерокалико-анастомоза справа
Рисунок 7. КТ урограмма того же больного через 6 месяцев после операции. Хорошая проходимость анастомоза
Обсуждение
В настоящее время методом выбора при первичных стриктурах ПУС является пиелопластика, которая может выполняться открытым, лапароскопическим и робот-ассистированным доступами [3, 6, 9-11]. При рецидивных протяженных стриктурах ПУС применяются лоскутные варианты пластики или уретерокаликоанастомоз, а при их неэффективности — аутотрансплантация почки, замещение мочеточника сегментом кишки или аппендиксом при его наличии или нефрэктомия [3, 6, 11]. Операция по Нейверту идеально подходит для пациентов с интрапочечной лоханкой, расширенной нижней чашкой и тонкой паренхимой над ней.
Лапароскопический уретерокаликоанастомоз был впервые описан в 2003 году [4]. Осложнений при операциях не было, но одному пациенту через 6 мес. произведена нефрэктомия, а другой чувствовал себя хорошо спустя 9 мес. В литературе встречаются результаты успешных лапароскопического и робот-ассистированного уретерокаликоанастомоза [7, 8, 12-13]. Arap M.A. et al. [12] выполнили подобную операцию у 6 пациентов. Другие авторы оперировали единичных больных [6-8, 11-13]. Интересным является клинический случай, описанный Kalathia J. et al. [14], которые выполнили анастомоз мочеточника с средней чашечкой тазоводистопированной почки.
Уретерокаликоанастомоз относится к редким операциям и основные этапы его выполнения независимо от доступа остаются одинаковыми. Важной технической особенностью данного вмешательства является то, что паренхима, расположенная в области нижней чашечки, должна быть резецирована, а не рассечена. Простая нефротомия над чашкой не может быть достаточной для последующего надежного формирования уретерокаликоанастомоза, так как неизбежны вторичные стриктуры в области соустья. Но, в отличие от открытой операции, при лапароскопическом и робот-ассистированном доступе наблюдаются меньшие кровопотеря и боль, низкий процент осложнений и быстрое послеоперационное выздоровление [68, 12-14].
Заключение
Лапароскопический уретерокаликоанастомоз при протяженной стриктуре прилоханочного отдела мочеточника является альтернативой открытой операции по Нейверту. Основными этапами данного вмешательства являются мобилизация мочеточника и нижнего полюса почки, резекция паренхимы над чашечкой и формирование широкого каликоуретероанастомоза.
Исследование не имело спонсорской поддержки. Авторы заявляют об отсутствии конфликта интересов.
Литература
Статья опубликована в журнале «Вестник урологии» №3 2017, стр. 87-94
Стриктура мочеточника
Стриктура мочеточника – это аномальное сужение канала мочеточника, полностью или частично нарушающее его проходимость. В результате нарушения оттока мочи из почки патология становится причиной развития различных заболеваний: пиелонефрита, камнеобразования, гидронефроза, хронической почечной недостаточности, сопровождающихся характерной симптоматикой. Диагностируют стриктуру мочеточника по результатам урографии, УЗИ, МРТ и КТ почек. Лечение оперативное, состоит в иссечении и пластике патологического участка, установке стента.
МКБ-10
Общие сведения
Стриктуры мочеточника могут возникать в разных отделах органа и иметь различную длину. Наиболее часто стриктуры наблюдаются на юкставезикальном (переход мочеточника в мочевой пузырь) и пиелоуретеральном (переход лоханки в мочеточник) участках. Патология может быть врожденной и приобретенной. Врожденные сужения выявляются у 0,6% детей, обычно носят односторонний характер. Самой распространенной специфической причиной приобретенных структур является туберкулез. Диагностику и лечение заболевания осуществляют специалисты в сфере практической урологии.
Причины
К врожденным стриктурам мочеточника относятся рубцовые изменения стенки протока из-за имеющихся наследственных аномалий, а также его сдавления при пересечении с кровеносными сосудами (например, добавочным почечным сосудом). Причинами приобретенной стриктуры являются:
При туберкулезе множественные рубцовые сужения формируются на участках подвергшихся инфильтрации и изъязвлениям. Пострадиационные стриктуры наблюдаются, как правило, в его тазовом отделе и могут быть связаны с проведением лучевой терапии при раке простаты, прямой кишки и женских половых органов. Сужения мочеточника после урологических оперативных вмешательств (уретеролитотомии, реконструкции лоханочно-мочеточникового сегмента) могут наблюдаться в любом отделе органа.
Патогенез
Имеющиеся в норме анатомические и физиологические сужения мочеточника при необходимости способны значительно расширяться благодаря его эластичной стенке. В отличие от них при стриктуре мочеточника происходят фиброзно-склеротические изменения, затрагивающие подслизистый, мышечный и наружный слои стенки мочеточника. В свою очередь это приводит к атрофии части мышечных элементов и их замещению на рубцовую ткань, гипертрофии поперечных мышечных волокон, а также к изменениям иннервации стенки.
Вследствие этого в области стриктуры отмечается стойкое уменьшение диаметра выводного протока, приводящее к нарушению нормальной функции мочеточника. На участках выше стриктуры из-за застоя мочи усиливается давление на мочеточник, наблюдается его растяжение, удлинение и извитость, возможно расширение лоханки и развитие гидронефроза (уретерогидронефроза).
Классификация
Истинная стриктура мочеточника по происхождению бывает врожденной и приобретенной. Сужения мочеточника могут быть односторонними и двухсторонними, одиночными и множественными, истинными (вследствие изменений, затрагивающих стенку) и ложными (по причине его компрессии извне).
Симптомы стриктуры мочеточника
Диагностика
Диагноз стриктуры мочеточника устанавливает врач-уролог по результатам УЗИ почек, УЗДГ сосудов, рентгеноконтрастного обследования, КТ почек и МРТ. Проведение трехмерной УЗ-ангиографии с диуретической нагрузкой позволяет одновременно увидеть расширенный отдел мочеточника выше стриктуры и оценить сосуды почек.
Рентгенконтрастная урография (экскреторная, инфузионная, ретроградная) дает возможность визуализировать ткани почек и мочевыводящие пути, определить сужение мочеточников, протяженность стриктур, оценить снижение выделительной способности почек. В сложных случаях применяют КТ или МРТ, дополнительно выявляющие заболевания смежных органов и тканей, оказывающих влияние на почки и мочеточники.
Лечение стриктуры мочеточника
Патология является абсолютным показанием для оперативного лечения, выбор которого определяется структурно-функциональным состоянием мочеточников и почек, протяженностью и уровнем стеноза. При минимальном поражении почечной ткани выполняют различные реконструктивные операции соответствующего отдела мочеточника, цель которых – ликвидировать сужение протока, восстановить свободный отток мочи из чашечно-лоханочного аппарата почек.
При серьезных поражениях верхних мочевых путей и развитии почечной недостаточности первым этапом оперативного лечения является открытая или пункционная нефростомия. Иногда производится эндоуретеральное рассечение спаек с установкой стента, бужирование и баллонная дилатация суженного отдела мочеточника, но они не дают стойкого эффекта и могут привести к еще большим осложнениям. Основные операции:
При стриктурах мочеточника, осложненных тяжелыми поражениями почечной ткани (поликавернозным туберкулезом, гидронефрозом, пионефрозом, сморщиванием почки) проводят нефроуретерэктомию (удаление почки и мочеточника).
Прогноз и профилактика
Для достижения благоприятного результата реконструктивно-пластические операции необходимо проводить на ранних стадиях до развития хронической почечной недостаточности. После реконструктивной пластики важную роль играет постоперационная реабилитация. Возможными осложнениями операций по поводу стриктур мочеточника является несостоятельность анастомозов, приводящая к забрюшинным мочевым затекам, развитию мочевой флегмоны, перитонита. Профилактика заключается в предупреждении и своевременном лечении заболеваний, способных стать причиной данной патологии.
Стриктура мочеточника
Стриктура мочеточника – это патологическое состояние частичного или полного сужения просвета мочеточника, приводящее к нарушению оттока мочи.
Анатомия
Мочеточник – это парный мочевыводящий орган, представляющий собой тонкую длинную трубку (две), соединяющую лоханку почки и мочевой пузырь. Мочеточник имеет три анатомических сужения, которые, при необходимости, благополучно расширяются благодаря эластичной стенке.
Но при стриктуре развиваются фиброзные изменения, по причине которых мышечные ткани стенки мочеточника замещаются на рубцовую ткань, которая не может расширяться и в месте сужения фиксируется уменьшение диаметра выводного протока. По этой причине над местом сужения моча собирается и застаивается, что приводит к растяжению мочеточника и появлению сопутствующих проблем с почками (расширение лоханки, гидронефроз и др.)
Участок стриктуры может быть коротким или длинным, может появляться в разных отделах мочеточника, но, как правило, «привычным» местом локализации стеноза является:
Осложнения стриктуры мочеточника
Поскольку при сужении мочеточник теряет свои функциональные свойства по причине стойкого уменьшения диаметра, развиваются различные патологические состояния:
Все эти факторы могут привести к серьезным осложнениям:
Причины развития стеноза мочеточника
Стриктура мочеточника может быть истинной (паталогические изменения стенки) и ложной (при сдавливании стенок мочеточника извне, например, опухолевыми образованиями).
Основные причины развития заболевания подразделяются на врожденные и приобретенные.
Врожденные причины – наследственные аномалии, с которыми человек родился:
Приобретенные причины – различные заболевания и поражающие воздействия:
Также стеноз мочеточника может быть односторонним и двусторонним, а также одиночным и многочисленным.
Симптомы стриктуры мочеточника
Чаще всего развивается односторонний процесс, который дает не такие яркие симптомы, как стеноз двусторонний. Как правило, заболевание имеет признаки, характерные для большинства заболеваний мочевыделительной системы:
Также могут проявляться интоксикационные симптомы: температура, озноб, слабость, мышечные судороги, тошнота, рвота.
Диагностика стриктуры мочеточника
Диагностика заболевания требует комплексного подхода и включает в себя, кроме осмотра и сбора анамнеза, следующие диагностические мероприятия:
Лечение стриктуры мочеточника
От стриктуры мочеточника можно избавиться только хирургическим путем – консервативное лечение, а тем более народные методы абсолютно неэффективны.
Выбор метода оперативного вмешательства зависит от общего состояния мочеточника и почек, количества и протяженности стриктур, стадии патологического процесса.
Профилактика стриктуры мочеточника
Процесс сужения мочеточника достаточно длительный, поэтому необходимо знать основные причины возникновения заболевания и по возможности стараться их избегать или быстро корректировать.
Гидронефроз и стриктуры мочеточника
Определение и классификация гидронефроза
Гидронефроз – это функциональное нарушение чашечно-лоханочной системы почки. В результате стеноза усложняется отток мочи и повышается гидростатическое давление. Такие изменения приводят к трансформации паренхимы, ухудшают работу почки. Различают три стадии: начальную, раннюю, терминальную. Нарушение чаще встречается у женщин.
Этиология и патогенез гидронефроза
Различают врожденный и приобретенный гидронефроз. Патология всегда сопровождается сужением ЛМС (лохано-мочеточникового сегмента), аномалию могут вызывать следующие факторы.
Сдавление и пульсовое воздействие со стороны добавочного нижнесегментарного артериального сосуда.
Отклонение в развитии семенных и почечных вен.
Сегментарная дисплазия ЛМС.
Педункулит из-за вытекания мочи в почечный синус.
К провоцирующим факторам относятся: подвижность почки, аномальная работа парапельвикальной клетчатки, дисфункция почечных кровеносных сосудов.
Клиническая картина гидронефроза
Различает два этапа. Первый характеризуется образованием обструкции ЛМС, симптоматика невыражена. Для второго характерны основные признаки почечной недостаточности:
тупая боль в области поясницы;
наличие крови в моче;
При обострении возможна картина почечной колики. Специфичным симптомом для гидронефроза является выбор больного спать на животе, поскольку перераспределение внутрибрюшного давления облегчает отток мочи.
Диагностика гидронефроза
Для постановки диагноза пациентам проводят клинико-лабораторные исследования. Кроме анализов мочи и крови используют инструментальные методы. Если необходима операция, обязательно проводят гистологический анализ пораженной ткани.
Физикальный осмотр
На ранних стадиях малоинформативен, заметить нарушение при пальпации и перкуссии возможно на последних этапах болезни.
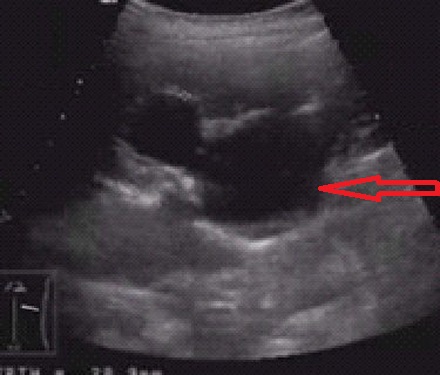
Ультразвуковое исследование
Ультразвуковое исследование. Диалатация чашечно-лоханочной системы.
При подозрении на данную патологию исследования проводят полипозиционно, оценивают состояние почки, лоханок, мочеточника, сосудов. Для корректного диагноза используют сравнение со здоровой почкой.
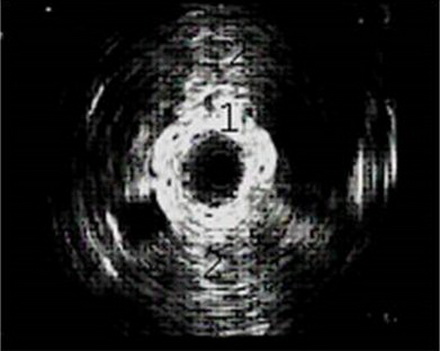
Эндолюминальная эхосонограмма зоны лоханочно-мочеточникового сегмента.
1. Стенка мочеточника.
2. Склероз парауретеральной клетчатки
Состояние парауретеральной клетчатки показывает эндолюминальный датчик, который заводят через мочеточник. Для оценки функциональных возможностей используют фармакоэкографию с мочегонными препаратами.
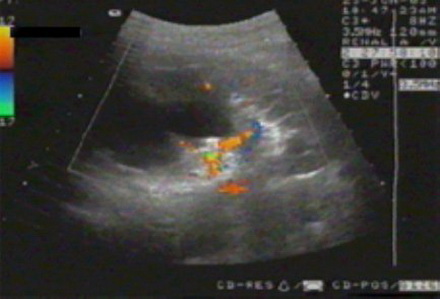
Эходоплерография сосудов почек.
Эходопплерограмма. Снижение интенсивности кровотока в области истонченной паренхимы верхнего и среднего сегментов почки.
Исследование актуально для оценки гемодинамических отклонений. Патология приводит к трансформации органа и растяжению артериальных и венозных сосудов. По их размерам можно судить о стадии и корректно выбирать лечение.
Рентгенологические методы обследования
Если нет противопоказаний, то рентгенологические исследования с контрастом являются приоритетными в диагностике гидронефроза.
Экскреторная урограмма. Стеноз лоаночно-мочеточникового сегмента, гидронефроз справа.
Благодаря рентгеноконтрастным препаратам метод дает оценку экскреторным функциям почек. Он эффективен на начальных стадиях заболевания, по мере нарастания патологии диагностическая эффективность снижается.
Применяется для обследования мочевых путей, показывает их структурное состояние, но не отражает функционального.
Применяется при непереносимости йодсодержащих контрастов. Актуальна для пациентов со значительным угнетением почечной функции. Результативность исследования повышает видеозапись.
Антероградная чрескожная пиелография.
Назначается, когда уретеропиелография невозможна и когда почка не выделяет контрастное вещество.
Диагностирует нарушения в развитии почек и сосудов. Для уровазального конфликта характерна патология наполнения ЛМС. Метод позволяет оценить трансформацию органа и прилегающих сосудов.
Мультиспиральная компьютерная томография. 3D реконструкция. Стеноз лоханочно-мочеточникового сегмента, гидронефроз справа.
Исследование неинвазивно и с высокой точностью показывает структурные изменения мочеполовой системы. На основании снимков проводится трехмерная реконструкция, что позволяет увидеть объем поражения и протяженность деформированного участка мочеточника. Не отражает функциональных изменений.
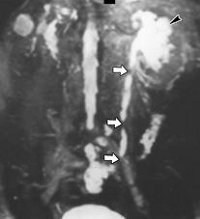
Магнитно-резонансная урография. Стеноз лоханочно-мочеточникового сегмента, гидронефроз справа.
Современный и наиболее информативный метод. Используется магнитно-резонансная урофагия с контрастом и без. В результате получают динамические изображения, которые демонстрируют все этапы эвакуации жидкости. Для более четкой визуализации мочевых путей используют фармакологические агенты. При большом количестве томографических срезов возможна 3D-реконструкция изображения.
Радионуклидные исследования
Для диагностики используют динамическую нефросцинтиграфию, в ходе которой оценивают транспорт радиоактивного вещества. Выделяют три сегмента исследования, каждый со своим временным течением. Первый отражает кровенаполнение почечных сосудов, второй – транспорт через клетки эпителия проксимальных канальцев, третий – уродинамику верхних мочевых путей. Метод показывает функциональные изменения, не дает информации о структурных деформациях.
Лечение гидронефроза
Сложность обнаружения патологии на начальных стадиях делает основным методом лечения реконструктивную операцию.
Подготовка к операции
Предусматривает комплекс мер по устранению патологических состояний и нормализации физиологических отклонений, что позволяет увеличить резерв функциональных возможностей почек. Для ликвидации воспалительного процесса используют НПВС, антигистамины, антибиотики. Для оздоровления соединительной ткани назначают солкосерил и вобэнзим.
Для снижения функциональной дегенерации назначают β2-адреномиметик гинипрал, на начальных стадиях это позволяет избежать операции. Также выполняется дренирование нефростомой или катетером-стентом.
Реконструктивные операции
Показаниями являются прогрессирование патологии, разрушение ткани, ведущее к функциональной и структурной гибели почки, сопутствующий гнойный пиелонефрит, состоявшееся почечное кровотечение.
Уретеропиелопластика (операция Андерсена-Хайнса) предусматривает резекцию больной зоны мочеточника и лоханки и создание пиелоуретерального анастомоза. Успешность операции обусловлена правильным определением зоны афункционального участка, резекция проводится на 5-6 мм дистальней пораженной ткани..
При стенозе ЛМС и наличии добавочного сосуда выполняется резекция, которая позволяет привести в соответствие просвет сосуда и паренхимы.
Важной частью вмешательства является эффективное дренирование, различают: нефростомию, установку мочеточникового катетера, катетера-стента. Важно предупредить воспалительные осложнения и внешнее инфицирование.
Включают два вида вмешательства: антеградную чрескожную эндопиелотомию и баллонную дилатацию. Операции показаны при небольших изменениях лоханки и отсутствии добавочного сосуда из-за высокого риска кровотечения. Эффективность составляет 72% против 89% открытого метода.
Сочетают в себе методы предыдущих двух. Позволяют проводить резекцию и наложение анастомоза, при этом характеризуются малой травматичностью и уменьшают сроки госпитализации
Послеоперационное ведение
Для нормального отведения мочи устанавливается катетер Фоли № 12-14. Чтобы уменьшить отек, назначают НПВС и уросептики. Для улучшения питания тканей используют венорутон, трентал. Для восстановления слизистой применяют вобэнзим и солкосерил. Длительность терапии в каждом случае определяется индивидуально, но ее срок составляет не менее 10 дней.
Антибиотики назначают после удаления дренажа с целью предупредить формирования мультирезистентной флоры, исключением является стойкое воспаление в первые сутки после операции.
После нефростомии обязательно проводят антеградную рентгенотелевизионную уроскопию и пиеломанометрию для проверки состоятельности верхних мочевых путей.
Заключение
Правильная диагностика и выбор метода коррекции определяют успешность терапии. Не менее важны предоперационная подготовка и послеоперационное обследование, оно позволяет определить успешность вмешательства, на ранних стадиях скорректировать осложнения.