Реинфекция что это такое
Значение слова «реинфекция»
Источник (печатная версия): Словарь русского языка: В 4-х т. / РАН, Ин-т лингвистич. исследований; Под ред. А. П. Евгеньевой. — 4-е изд., стер. — М.: Рус. яз.; Полиграфресурсы, 1999; (электронная версия): Фундаментальная электронная библиотека
РЕИНФЕ’КЦИЯ, и, ж. [от латин. приставки re — опять, снова и слова инфекция] (мед.). Повторное заражение, повторная инфекция.
Источник: «Толковый словарь русского языка» под редакцией Д. Н. Ушакова (1935-1940); (электронная версия): Фундаментальная электронная библиотека
Делаем Карту слов лучше вместе

Спасибо! Я обязательно научусь отличать широко распространённые слова от узкоспециальных.
Насколько понятно значение слова планетный (прилагательное):
Синонимы к слову «реинфекция»
Предложения со словом «реинфекция»
Понятия, связанные со словом «реинфекция»
Отправить комментарий
Дополнительно
Предложения со словом «реинфекция»
Важно заметить, что врождённого и приобретённого иммунитета к гонорее нет, поэтому после перенесения заболевания возможно повторное его развитие, причём обычно реинфекция протекает так же остро, как и в случаях первичного заражения.
Поскольку нередко встречаются случаи реинфекции (повторного инфицирования), вызывающие клинически выраженные формы заболевания, очевидно, что развивающийся после однократного эпизода инфекции иммунитет недостаточно напряжённый или продолжительный.
Повторное заболевание вследствие заражения тем же инфекционным агентом называют реинфекцией.
РЕИНФЕКЦИЯ
РЕИНФЕКЦИЯ (лат. re- приставка, означающая повторение, возобновление, + позднелат. infectio заражение)— повторное заражение тем же видом возбудителя, что и при первом заболевании, вновь вызвавшее инфекционный процесс.
Р. чаще развивается в тех случаях, когда первичный инф. процесс не оставляет после себя достаточно напряженного и продолжительного иммунитета (см.), напр, после перенесенной дизентерии (см.), сальмонеллеза (см.), или при частичной утрате иммунитета, напр, против тифопаратифозных заболеваний (см. Брюшной тиф).
Различают гомологичную и гетерологичную Р. Если повторный инф. процесс возникает вследствие нового заражения возбудителем того же вида, что и первичный, говорят о гомологичной (истинной) Р. Под гетерологичной Р. понимают повторное развитие инф. процесса при попадании в организм возбудителя другого подвида или серотипа, напр, после перенесенной дизентерии, вызванной шигеллой Флекснера подвида Ньюкасла, развивается дизентерия, вызванная шигеллой Флекснера подвида Бойда.
В связи с тем, что иммунный ответ организма достаточно выражен против определенного вида возбудителя и при этом более длительно сохраняется достаточная напряженность клеточного и гуморального иммунитета, гомологичная Р. наблюдается значительно реже, чем гетерологичная, и обычно не ранее чем через один год после первичного инф. процесса.
Дифференцируют гомологичную Р. с гетерологичной с помощью серол. метода идентификации бактерий возбудителей инфекции (см. Серологические исследования).
Клин, проявления реинфекции, как правило, бывают менее выражены, чем при первичном инф. процессе.
Библиография: Многотомное руководство по микробиологии, клинике и эпидемиологии инфекционных болезней, под ред. H. Н. Шукова-Вережникова, т. 4, с. 32, М., 1964; Покровский В. И. и д р. Приобретенный иммунитет и инфекционный процесс, М., 1979.
Повторные респираторные инфекции у детей (часто болеющие дети)
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Отечественная педиатрическая наука продолжает оперировать таким термином, как «часто болеющие дети» (ЧБД). В составе этой группы оказываются дети с повторными инфекциями верхних дыхательных путей. Таким образом, состояние, констатация факта повторных инфекций начинают восприниматься как диагноз. Восприятие явления повторных инфекций как диагноза нередко приводит к неоправданной полипрагмазии, отвлечению сил и средств медицинской службы от действительно больных детей. Часто действия врача по отношению к ЧБД оказываются эмпирическими и основываются на бездоказательных рекомендациях. Во избежание подобного роль дифференциальной диагностики и понимание полиэтиологичности заболевания для правильного выбора терапии становятся еще более значимыми.
Острые респираторные инфекции (ОРИ), или простудные заболевания, назофарингит, ринофарингит – инфекции верхних дыхательных путей с первичным и преимущественным поражением носа, сопровождающиеся кашлем, ринореей, конъюнктивитом, болями в горле, лихорадкой, разрешающиеся в подавляющем большинстве случаев самостоятельно в ближайшие 7–10 дней. Некоторые признаки могут сохраняться до 3 нед. Инфекции уха, горла, носа, а также бронхолегочные инфекции составляют основной перечень заболеваний в детском возрасте [1, 2]. Дети первых 5 лет жизни, посещающие дошкольные учреждения, переносят до 8 эпизодов ОРИ в год при полностью сохранном иммунитете [3, 4]. Сезонное увеличение числа случаев респираторных инфекций, которые в России, Европе и США традиционно трактуются как простудные (common cold), известно даже в тропиках в сезон дождей, и там точно также обсуждается та же самая проблема врачебной тактики [5].
Существует более 250 инфекционных агентов, вирусов и бактерий, вызывающих респираторные заболевания. Самый частый возбудитель ОРИ (до 80%) – риновирус, вариант пикорнавируса, насчитывающий более 90 серотипов. Часто выявляются коронавирусы, вирусы гриппа (10–15%), парагриппа, аденовирусы (5–7%), респираторный синцитиальный вирус, метапневмовирус и другие. Нередко у обследованных выявляется два и более вируса. Спектр инфекционных агентов достаточно стабилен, и частотное соотношение возбудителей ОРИ, обнаруженных независимыми исследователями в разных странах Европы и даже Африки, весьма сильно совпадает [6].
Чем теснее контактируют люди (детские сады, школа, общежития, перенаселенная квартира, транспорт мегаполисов), тем быстрее распространяется инфекция. Получена положительная корреляционная связь между длительностью пути на работу и респираторной заболеваемостью. ОРИ традиционно называются и трактуются как простудные заболевания. Но холод сам по себе не вызывает респираторных заболеваний. Их причина – вирусы или бактерии. Подъем заболеваемости в холодное влажное время года объясняют длительным нахождением аэрозольных капель во влажном воздухе, местными изменениями респираторного тракта в ответ на холод, сниженным иммунным ответом, длительным нахождением детей в помещении и началом занятий в школе.
Но в практических условиях педиатр всегда стремится исключить сложные заболевания, протекающие под маской рецидивирующих респираторных инфекций. Такие дети нередко направляются на консультативные приемы с подозрением на иммунодефицит (ИД).
Следует различать физиологическую и патологическую склонность к инфекции. В физиологических состояниях ребенок, даже переносящий повторные респираторные инфекции, растет и развивается нормально, будучи выведен из привычного коллектива на дачу, каникулы, перестает болеть. В семейном анамнезе нет родственного брака. Перенесенная инфекция оставляет иммунитет и защищает от реинфекции этим же вирусом. Живые вакцины не приводят к поствакцинальным инфекциям. Нет системных инфекций, нет персистенции инфекции и атипичных возбудителей, выздоровление – без дефекта. Вилочковая железа, миндалины, аденоиды, лимфатические узлы в период инфекции увеличиваются в размерах [7].
Для ИД [8] характерно необычное течение инфекций (высокая частота, затяжное и осложненное течение, оппортунистическая инфекция и т.д.). И при таком развитии заболевания часто рассматривается применение иммуномодулирующих препаратов. Но возможно необычное течение инфекций без признаков ИД. Это типично для следующих синдромов:
• нарушение кровообращения, в т.ч. на уровне микроциркуляции, врожденные и приобретенные пороки сердца и магистральных сосудов, тяжелые хронические анемии, сахарный диабет;
• обструкции полых органов: стенозы мочеточника или уретры, бронхиальная астма, бронхоэктазы, муковисцидоз, синдром нарушенного мерцания ресничек, нарушение проходимости евстахиевой трубы (анатомические вариации, аденоидные вегетации);
• дефекты питания и состояния с потерей белка, стрессы, мальнутриция любого генеза, нефротический синдром, белковотеряющая энтеропатия, экзема, ожоги, переломы больших костей;
• инородные тела: шунты вентрикулярные при гидроцефалии, внутрисосудистые стенты, катетеры, искусственные клапаны сердца, водители ритма, аспирированные или забытые при операциях инородные тела;
• необычная манифестация собственно микробного фактора: рост необычной флоры после ятрогенной элиминации привычных возбудителей, хроническая инфекция устойчивыми микроорганизмами, постоянная реинфекция (употребление зараженных продуктов или воды, пребывание в зараженной атмосфере птичников, зооферм, лабораторий и т.д., постоянный контакт с человеком или животным – носителями инфекции; контаминированные кондиционеры, ингаляторы и медицинский инструментарий).
Отправными пунктами для диагностики и дифференциальной диагностики первичных ИД являются рецидивирующие инфекции, их высокая частота, краткие или вообще отсутствующие бессимптомные промежутки, резистентность инфекции к терапии, необычное течение болезни или необычная инфекция, труднообъяснимые или тяжелые осложнения [9, 10]. Разработаны 10 настораживающих признаков первичных иммунодефицитных состояний:
1. Наличие у родственников больного первичных ИД, ранних смертей от тяжелых инфекций или одного из нижеперечисленных состояний.
2. Отставание грудного ребенка в весе и росте.
3. Персистирующая молочница или грибковое поражение кожи в возрасте старше 1 года.
4. Заболевания отитом не менее 6–8 раз за год.
5. Несколько подтвержденных серьезных синуситов (не менее 4–6 раз в течение года).
6. Более двух подтвержденных пневмоний.
7. Повторные глубокие абсцессы кожи и внутренних органов.
8. Потребность в длительной терапии антибиотиками для купирования инфекции (до 2 мес. или дольше).
9. Потребность во внутривенной антибиотикотерапии для купирования инфекции.
10. Не менее двух таких инфекций, как менингит, остеомиелит, сепсис.
Если у пациента обнаружено 2 и более только что перечисленных признаков, то диагноз ИД вероятен.
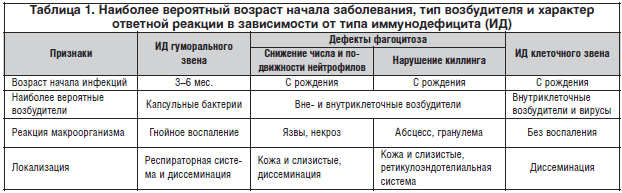
Для правильной диагностики имеют значение возраст дебюта патологии, общий статус пациента, преимущественная топическая локализация инфекции, ее вид и ответная реакция макроорганизма [11]. При первичных ИД, кроме В-иммунодефицита, нередко отмечается задержка умственного развития. Тип инфекции достаточно характерен для определенного вида ИД. Пневмококки и стрептококки излюбленно поражают людей с В-клеточным (антительным) дефицитом. Тяжелые вирусные, грибковые и другие оппортунистические инфекции указывают на Т-клеточный дефицит. Возвратные инфекции грамотрицательной флорой и стафилококками нередко сопровождают детей с нарушенным фагоцитозом, а Neisseria – с дефицитом компонентов комплемента (табл. 1). Типирование возбудителя должно строиться непосредственно на его выявлении, т.к. иммунологические методы в условиях невозможности антительного ответа или клеточной реакции могут дать ложноотрицательные результаты. Лабораторная диагностика ИД проводится по этапам (табл. 2):
1 этап – поликлинический и общие лечебные учреждения;
2 – специализированные учреждения.
Среди детей дошкольного возраста, наблюдаемых как часто болеющие респираторными вирусными инфекциями, до 30–40% составляют дети с бронхиальной астмой легкого течения [12]. Подтверждением этого является то, что большая группа т.н. ЧБД в поликлиническом звене нередко имеет в индивидуальных картах такие сопутствующие состояния, как «респираторный аллергоз», «обструктивный бронхит» и т.д. Поэтому при исключении случаев физиологической реакции на инфекцию следует помнить о возможной бронхиальной астме. Повторные ОРИ, наслаиваясь на аллергически воспаленную слизистую, способны у генетически предрасположенных людей вызывать гиперреактивность бронхов. Признаками респираторной аллергии могут быть только хронический ринит и кашель как эквивалент астмы. Респираторную аллергию следует исключать при наличии следующих признаков:
1. респираторные симптомы не сопровождаются лихорадкой. Отделяемое из носа водянистого характера;
2. регистрируются признаки атопии;
3. в индивидуальном анамнезе есть указания на атопический дерматит или непереносимость отдельных видов пищи;
4. в семейном анамнезе есть случаи атопического дерматита, экземы, аллергического ринита или астмы;
5. ухудшение состояния развивается сезонно или после экспозиции с определенным веществом, растением или животным;
6. антибиотики малоэффективны;
7. облегчение приносят антигистаминные препараты и бронходилататоры.
В случае исключения органических причин повторных респираторных инфекций встает проблема выбора оптимальной терапии, сочетающей эффективность и безопасность при общей доступности.
При определении тактики ведения детей с повторными случаями ОРИ необходимо исключить наличие аденоидитов, тонзиллофарингитов, требующих соответствующего лечения. После этого дискутируется возможность назначения иммуномодулирующей терапии. Наиболее часто применяемые в детской практике иммуномодуляторы относятся к препаратам синтетического и бактериального происхождения. Единственным лекарственным препаратом природного происхождения является натрия нуклеинат.
Этот биопрепарат имеет хорошую доказательную базу. Так, in vitro натрия нуклеинат продемонстрировал возможность снижения продукции провоспалительных цитокинов мононуклеарами периферической крови человека (IL-6, ИФ-γ), а также оказался эффективным ингибитором LPS-индуцированного сепсиса в экспериментах in vivo [17]. Кроме того, дальнейшее изучение натрия нуклеината выявило его способность увеличивать противовоспалительную функциональную активность моноцитов/макрофагов за счет регулирования синтеза активных форм кислорода [18]. В эксперименте также показана способность натрия нуклеината снижать активность процесса хронического воспаления, улучшая гистологические показатели его течения [15].
Длительность применения препарата в клинике с возможностью анализа его эффективности при различных состояниях позволила сделать оптимистические выводы [13, 14]. Назначение натрия нуклеината часто болеющим пациентам приводит к повышению качества жизни, общей активности, работоспособности, снижению утомляемости с положительным иммуномодулирующим и иммунопрофилактическим эффектом. Препарат назначался по 2 капсулы 2 раза/сут. и не вызывал побочных действий [16].
Помимо иммуномодулирующей терапии требуются режимные мероприятия, связанные с закаливанием, регуляцией контактов.
Таким образом, проблема часто и длительно болеющих детей является весьма актуальной. Требуется исключение состояний, имитирующих банальные респираторные инфекции и требующих специализированной помощи. Тактика врача определяется преморбидным состоянием ребенка, наличием аденоидита, тонзиллофарингита. В лечении наряду с общеукрепляющими процедурами обсуждается применение иммуномодулирующих препаратов как синтетического, так и природного происхождения.
Литература
1. Доклад о состоянии здоровья населения Москвы в 2008 г. / Правительство Москвы. Департамент здравоохранения. Управление Роспотребнадзора по городу Москве. М., 2009. 174 с.
2. Доклад о состоянии здоровья населения Москвы в 2009 г. / Правительство Москвы. Департамент здравоохранения. Управление Роспотребнадзора по городу Москве. М., 2010. 172 с.
3. Альбицкий В.Ю., Баранов А.А. Часто болеющие дети. Клинико-социальные аспекты. Пути оздоровления. Саратов, 1986. 165 c.
4. Rieger C., Hardt H. (Hrsg.) Padiatrische Pneumologie. Springer, Berlin, 1999. 1157 s.
5. Perera B. Bacterial immunostimulants in recurrent pediatric respiratory infections // Sri Lanka Journal of Child Health, 2011. Vol. 40. P. 43–44.
6. Siegenthaler W. (Hrsg.) Differentialdiagnose innnerer Krankheiten. 17. neubearbeitete Auflage. Stuttgart: Geirg Thieme Verlag, 1993.
7. Slatter M., Gennery A. Clinical Immunology Review Series: An approach to the patient with recurrent infections in childhood // Clin. Experim. Immunol. 2008. Vol. 152. P. 389–396.
8. Кондратенко И.В., Бологов А.А. Первичные иммунодефициты. М.: Медпрактика-М, 2005. 232 с.
9. Champi C., Primary immunodeficiency disorders in children: prompt diagnosis can lead to lifesaving treatment // J. Pediatr. Health Care. 2002. Vol. 16. P. 16–21.
10. Rich R., Fleisher Th., Shearer W. et al. (Ed.) Clinical immunology. Principles and practice. London: Mosby, 2003. Vol. 1, 2.
11. Beers M., Berkow R. (Eds.) The Merck Manual of Diagnosis and Therapy. 17-th Edition, 1999. 2833 p.
12. Зиновьева Н.В., Давыдова Н.В., Щербина А.Ю. и др. Часто болеющие дети: чем они больны на самом деле // Трудный пациент. 2007. № 2. С. 40–43.
13. Земсков А.М., Передерий В.Г., Земсков В.М. и др. Иммунокорригирующие нуклеиновые препараты и их клиническое применение. Киев: Здоровье, 1994. 232 с.
14. Катеруша Е.И. Клинико-иммунологические особенности и эффективность иммунотерапии у больных рецидивирующими формами зоба: автореферат дисс… к.м.н. Саратов, 2012. 28 с.
15. Шевченко А.Н., Коваленко Л.И. Клеточно-тканевая динамика воспаления на фоне введения натрия нуклеината // Український морфологічний альманах. 2011. Т. 9, № 4. С. 149–151.
16. Семидоцкая Ж.Д., Чернякова И.А., Бездетко Т.В. и др. Опыт применения нуклеината в лечении длительно и часто болеющих пациентов // Новости медицины и фармации. 2007. № 16.
17. Jukic T., Abidov M., Ihan A. A. tetrahydrophthalazine derivative «sodium nucleinate» exerts a potent suppressive effect upon LPS-stimulated mononuclear cells in vitro and in vivo // Coll Antropol. 2011 Dec; 35 (4):1219–23.
18. Jukic T., Ihan A., Jukic D. Tetrahydrophthalazine derivative «sodium nucleinate» exert its anti-inflammatory effects through inhibition of oxidative burst in human monocytes // Coll Antropol. 2012 Jun; 36 (2): 409–12.
Проблемы лечения вирусно-бактериальных респираторных инфекций у «часто и длительно болеющих» иммунокомпрометированных детей
Высокая частота заболеваемости детей повторными острыми респираторными инфекциями вирусного и/или бактериального происхождения всегда являлась весьма серьезной проблемой. Таких пациентов принято называть «часто и длительно болеющими» (ЧДБ). ЧД
Высокая частота заболеваемости детей повторными острыми респираторными инфекциями вирусного и/или бактериального происхождения всегда являлась весьма серьезной проблемой. Таких пациентов принято называть «часто и длительно болеющими» (ЧДБ). ЧДБ — это не нозологическая форма. Использование в педиатрии этой терминологии призвано акцентировать внимание клиницистов различных специальностей, в первую очередь, педиатров, оториноларингологов, пульмонологов, на проблемах детей, имеющих излишне частые (повторные) острые респираторные вирусно-бактериальные инфекции (ОРЗ, ОРВИ) различной этиологии. Многочисленными авторами показано сохранение неуклонного роста числа детей, принадлежащих к группе ЧДБ, составляющих 20–65% детской популяции, при этом отмечается резистентность (неотвечаемость) данной категории больных к традиционным методам терапии. На ЧДБ детей приходится 50–60% всех регистрируемых заболеваний. Около 20% ЧДБ детей болеют ОРЗ практически ежемесячно. В 40% случаев к 7–8 годам у ЧДБ детей формируется хроническая патология, при этом риск хронизации прямо пропорционален увеличению кратности эпизодов ОРЗ в течение года.
ОРВИ у ЧДБ детей нередко характеризуются затяжным течением и присоединением осложнений в виде обострений хронических очагов бактериальной инфекции ЛОР-органов, респираторного и урогенитального тракта. В ряде случаев пациенты из группы ЧДБ нуждаются в помощи клинического иммунолога, поскольку имеют серьезные нарушения функционирования иммунной системы и интерферонового статуса. Таким пациентам, как правило, показана адекватная иммунодиагностика, исследование интерферонового статуса, микробиоценоза слизистых (ПЦР, бакпосевы) с последующим проведением интерфероно- и/или иммунотерапии, санации хронических очагов инфекции на фоне диагностического мониторинга.
Наиболее часто педиатрами для формирования групп детей ЧДБ используются возрастные критерии, предложенные Барановым А. А. и Альбицким В. Ю. (1986): на первом году жизни — 4 и более острых и обострений хронических заболеваний в год, на втором-третьем годах жизни — 6 и более ОРЗ в год, на четвертом году — 5 и более, на пятом-шестом годах — 4 и более, на седьмом году жизни и старше — 3 и более ОРЗ в течение года.
В то же время необходимо отметить, что по нашим данным к ЧДБ взрослым пациентам относятся лица, страдающие ОРЗ более 2–3 раз в году, и в ряде случаев длительность заболеваний может колебаться от 7 до 14 и более дней (Нестерова И. В., Малиновская В. В. и соавт., 2005). При этом нами отмечено, что более чем в 50% случаев взрослые субъекты из числа ЧДБ в детстве также относились к группе ЧДБ. Примерно половина из них имела ремиссию в течение 4–6 лет, в которую они выходили, как правило, в период полового созревания. В последующем возврат к частым ОРЗ происходил на фоне различных провоцирующих факторов: тяжелый психоэмоциональный и/или физический стресс, оперативные вмешательства, наркоз, травмы, тяжелый грипп, ветряная оспа, перенесенная в возрасте старше 18 лет, использование больших доз глюкокортикоидов, неспецифических противовоспалительных препаратов и т. д. Эти наблюдения, по всей видимости, свидетельствуют об имеющихся в ряде случаев генетически обусловленных дисфункциях иммунной системы и системы интерферонов у лиц ЧДБ. В то же время манифестацию повторных ОРЗ необходимо рассматривать как проявление «индикаторных инфекций» ассоциированных с недостаточностью функционирования системы интерферонов (ИФН) и иммунной системы — иммунодефицитов, первичного или вторичного характера. Как правило, у детей или взрослых субъектов, имеющих сочетание ряда факторов риска, возможность реализации генетической предрасположенности к частым заболеваниям возрастает. Формирование контингента ЧДБ, детей и взрослых, во многом определяется неадекватностью реагирования иммунной системы и системы интерферонов на различные неблагоприятные воздействия, приводящие к развитию вторичной иммунной недостаточности (Нестерова И. В., 2008).
Именно с персистенцией вирусных и бактериальных антигенов, возникающей на фоне нарушений иммунитета и в то же время их усугубляющей, в последние годы связывают рецидивирующее течение респираторных заболеваний. Причем у 40–60% детей ОРЗ имеют вирусную природу. Среди вирусов ведущее место занимают риносинцитиальные (РС) вирусы, аденовирусы, риновирусы, вирусы гриппа и парагриппа. При неосложненном течении ОРЗ главенствующая роль отводится, как правило, моновирусной инфекции. Элиминация вирусных антигенов значительно затрудняется при частых рецидивах ОРЗ, особенно при наличии вторичной иммунной недостаточности. Так, вирусы гриппа, парагриппа, РС-вирусы, риновирусы, аденовирусы удается идентифицировать в течение продолжительного времени после острого периода болезни — от 2 недель до нескольких месяцев. От 10% до 30% ОРЗ у детей имеют бактериальное происхождение. Из бактериальных возбудителей, вызывающих острые заболевания органов дыхания, доминирующая роль принадлежит пневмококкам, гемофильной палочке. Однако развитие бактериального процесса может быть обусловлено и такими условно-патогенными микроорганизмами, как золотистый стафилококк, клебсиелла, представителями семейства кишечных палочек.
Особую настороженность вызывает возросшая частота заболеваний дыхательных путей, вызванных хламидиями, микоплазмами, уреаплазмами. Эти внутриклеточные паразиты способны к длительной персистенции в клетках эпителия респираторного тракта, особенно у иммунокомпрометированных детей, что и служит причиной инициации бронхообструктивного синдрома, а в дальнейшем формирования хронических воспалительных заболеваний легких, в том числе бронхиальной астмы.
Этиологическая значимость вирусно-бактериальных ассоциаций установлена в 25–30% острых заболеваний респираторного тракта. Клинически смешанная инфекция обусловливает неосложненное и осложненное течение ОРЗ. В случаях развития у детей острого воспалительного процесса нижних дыхательных путей смешанной этиологии вирусный компонент обычно предшествует бактериальному. Наслоение микробной инфекции нередко связывают с агрессией аутофлоры. При повторных ОРЗ, наряду с инфицированием новыми микроорганизмами, происходит активация латентной, персистирующей инфекции вирусного и бактериального генеза, что утяжеляет течение болезни, способствует хронизации процесса.
Ведущими отличительными признаками в клинической картине у ЧДБ детей являются: 1) резистентность (неотвечаемость) к традиционной терапии ОРЗ вирусной или бактериальной этиологии в соответствии с российскими формулярами; 2) проводимое традиционное лечение не предотвращает упорного рецидивирования (повтора) респираторных инфекций; 3) частота повторных инфекций превышает допустимый возрастной уровень и колеблется от 4–6–10 до 12–24 и более в год; 4) длительность ОРЗ превышает 7 дней и может колебаться от 8 до 14 и более дней; 5) ОРЗ вирусной этиологии провоцируют обострение хронических очагов бактериальной инфекции: хронического тонзиллита, хронических риносинуситов, хронического фаринготрахеита, хронического обструктивного бронхита и т. д.; 6) ОРЗ вирусной этиологии осложняется повторными пневмониями, резистентными к традиционной терапии.
Иммунная система (ИС) обеспечивает контроль за поддержанием антигенного гомеостаза в течение всей жизни человека, т. е. контроль как за проникновением чужеродных микроорганизмов и вирусов, так и генетической однородностью клеточных популяций самого организма. Главная функция иммунной системы: иммунологический надзор — распознавание «своего» и «не своего» (чужого), сохранение «своего» и мгновенное уничтожение «чужого». Таким образом, реализуется важнейший феномен иммунитета — феномен защиты организма от проникновения и негативного влияния любых чужеродных субстанций. В реализации реакций иммунной системы принимают участие два важнейших механизма: врожденный иммунитет и адаптивный (приобретенный) иммунитет.
Респираторные вирусы — облигатные внутриклеточные паразиты. Они различаются по своему строению и способам размножения. Одни из них вызывают острые инфекции и достаточно быстро элиминируются из организма хозяина, другие способны к персистенции.
К основным механизмам противовирусной защиты респираторного тракта относят: локальный иммунитет слизистых респираторного тракта (секреторный IgA, ИФН альфа, ИФН бета, провоспалительные цитокины, секретируемые эпителиальными клетками респираторного тракта), систему ИФН (ИФН альфа, ИФН бета, ИФН гамма), естественные киллерные клетки (CD3 + CD16 + CD56 + ), Т-клеточное звено иммунитета (CD3 + CD8 + ; CD3 + CD56 + ; CD8 + CD25 + ; CD3 + CD4 + ; CD8 + HLA-DR; CD4 + CD25 + ), гуморальные механизмы (нейтрализующие противовирусные антитела класса IgG). В настоящее время известно три основных типа ИФН: ИФН альфа, ИФН бета, ИФН гамма. В инфицированных вирусами клетках респираторного эпителия возрастает продукция ИФН альфа и ИФН бета. Эффекты ИФН альфа и ИФН бета: 1) активация противовирусных механизмов в неинфицированных клетках респираторного эпителия — протективный эффект, клетки приобретают невосприимчивость к вирусной инфекции; 2) активация генов с прямой противовирусной активностью. Антивирусные эффекты ИФН альфа и ИФН бета развиваются через несколько часов и длятся 1–2 дня.
Формирование иммунной системы и становление противовирусного иммунитета является результатом реализации генетической программы онтогенеза, для полноценного завершения которой необходима внешняя и внутренняя антигенная стимуляция. В этом аспекте неизбежные инфекции респираторного тракта у детей раннего возраста должны вести к иммунному тренингу организма. Склонность детей, особенно первых лет жизни, к ОРЗ отчасти обусловлена возрастными особенностями развития их ИС, в том числе и местного иммунитета. В свою очередь, слишком частые ОРЗ не могут негативно не влиять на становление ИС растущего организма, так, постоянная вирусно-бактериальная стимуляция ИС у детей ЧДБ ведет к возникновению нарушений ее функционирования, что сопровождается формированием стойкой иммунной недостаточности — вторичного иммунодефицита (ВИД). ВИД может быть представлен нарушениями как общего, так и местного иммунитета и носить комбинированный или изолированный характер.
В таблице приведена частота встречаемости нарушений различных механизмов противовирусного иммунитета у ЧДБ детей.
С целью повышения функциональной активности ИС, системы ИФН и ускорения восстановления их нарушенных функций, направленных на элиминацию вирусных и бактериальных антигенов, необходимо проведение заместительной и/или модулирующей иммунотерапии, восстанавливающей и модулирующей силу иммунного ответа, что должно обеспечить адекватный иммунный ответ на присутствие инфекционного патогена с последующей его элиминацией.
Тактика иммунотропной терапии при ВИД с синдромом вирусных и вирусно-бактериальных инфекций отличается тем, что в основе восстановления системы интерферонов и иммунной системы лежит базисная терапия отечественным рекомбинантным ИФН альфа-2 — Вифероном. Далее проводится необходимая иммунотерапия заместительного или модулирующего характера. При этом тактика иммунотерапии и, в первую очередь, ее длительность зависят от вида ВИД — острого или хронического. У детей ЧДБ, как правило, имеет место хронический или персистирующий ВИД, т. е. нарушения функционирования системы ИФН и иммунной системы существуют достаточно длительное время — от 6 месяцев до нескольких лет. Безусловно, при такой ситуации, в отличие от острых ВИД, когда иммунотерапия может занимать от 10 до 14 дней, проведение иммунотерапии в рамках программы иммунореабилитации детей ЧДБ занимает от 2,5–4,5 месяцев, в редких случаях до 2–3 лет.
Разработанная нами программа иммунореабилитации (Нестерова И. В., 1992) включает следующие положения:
Иммунотерапия, заместительного и модулирующего характера, органично включается в программы иммунореабилитации. К лекарственным препаратам, используемым для заместительной иммунотерапии, относятся внутривенные иммуноглобулины IgG и IgM обогащенные (Интраглобин и Пентаглобин), специфические иммуноглобулины против цитомегаловирусной инфекции (Цитотект), интерфероны (комплексный препарат рекомбинантного ИФН альфа-2 с антиоксидантами — Виферон в различных дозировках), тимические факторы (Тимоген, Тактивин).
Иммуномодулирующая терапия — «золотой стандарт» иммунотерапии. Результатом ее влияний при ВИД с инфекционным синдромом является восстановление работы дефектных звеньев иммунной системы, нивелирование гиперэргических реакций, восстановление адекватности реагирования иммунной системы на имеющиеся воспалительные процессы различной этиологии.
Одним из обязательных условий проведения иммуномодулирующей терапии при ВИД с вирусно-бактериальным инфекционным синдромом является выполнение ее в рамках традиционного лечения. При этом на начальных этапах в зависимости от вида инфекционного синдрома иммуномодулирующая терапия должна обязательно сочетаться с антибактериальной, противовирусной и/или противогрибковой терапией (Нестерова И. В., 2008).
С нашей точки зрения иммуномодулирующая терапия, используемая в лечении ЧДБ детей, должна иметь направленный характер: точкой приложения используемого иммуномодулирующего препарата должно являться то или иное поврежденное звено иммунной системы. При этом используется преимущественная направленность влияния(ний) иммуномодулятора. Так, для восстановления Т-клеточного звена предпочтительным является применение Тактивина, Тимогена, Имунофана, для восстановления гуморального звена, ЕКК, НГ Ликопида и Полиоксидония. Для восстановления системы ИФН — Виферона, который при определенных условиях обладает и иммуномодулирующими свойствами, направленными на восстановление Т-клеточного звена, системы нейтрофильных гранулоцитов. Для иммунопрофилактики и иммунотерапии бактериальных инфекций у детей ЧДБ может проводиться пролонгированная (в течение 5–6 месяцев) терапия топическими иммуномодуляторами — низкоиммуногенными вакцинами (ИРС 19, Имудон, Рибомунил, Бронхо-мунал и т. д.).
Интерферонотерапия с использованием Виферона обладает не только интерферонкорригирующей, иммуномодулирующей, но и противовирусной активностью и в большинстве случаев при возникновении ОРВИ может использоваться локально и системно, без синтетических противовирусных препаратов. Синтетические противовирусные препараты (Арбидол, Ремантадин) лучше использовать в остром периоде ОРВИ при среднетяжелом или тяжелом течении. При необходимости синтетические противовирусные препараты хорошо сочетаются с Вифероном. Хорошо известным фактом является повреждение клеточных мембран, наблюдаемое в ходе развития инфекционного процесса, что по данным В. В. Малиновской (1998) служит основной причиной снижения противовирусной активности интерферона. С целью восстановления взаимоотношений между антиокислительной активностью плазмы крови и перекисным окислением липидов в состав препарата Виферон введены токоферола ацетат и аскорбиновая кислота — антиоксиданты, являющиеся мембраностабилизирующими компонентами. В сочетании с ними противовирусная активность рекомбинантного ИФН альфа-2 возрастает в 10–14 раз, при этом отсутствуют побочные эффекты (повышение температуры тела, лихорадка, гриппоподобные явления, психогенная депрессия), возникающие при парентеральном введении препаратов других природных и рекомбинантных ИФН. Ректальное введение Виферона и комбинация с антиоксидантами, по-видимому, обеспечивают эти позитивные эффекты, также как и быструю высокую концентрацию и длительную циркуляцию в крови ИФН альфа-2. Следующим позитивным моментом является установленный факт: при применении Виферона в течение двух лет не выявлены антитела, нейтрализующие противовирусную активность рекомбинантного ИФН альфа-2. Особенности лекарственной формы Виферона — мазь, гель, ректальные суппозитории в различных дозах создают возможность проведения локальной и системной интерферонотерапии.
Нами разработаны основные принципы дифференцированной терапии Вифероном при вторичных ВИД с синдромом повторных ОРВИ, т. е. для детей ЧДБ (Нестерова И. В., 2003; 2005; 2007):
Ниже приведена разработанная нами ранее программа терапии Вифероном для детей ЧДБ с повторными ОРВИ:
Общая продолжительность курса 2,5–3,5 месяца.
NB! При необходимости (значительное снижение уровней индуцированного ИФН альфа!) начальная доза Виферона может увеличиваться в 1,5–2 раза, а курс лечения продлеваться до достижения позитивного клинического эффекта.
Использование описанных выше подходов в лечении детей ЧДБ позволяет получать позитивные результаты, которые можно видеть при оценке клинической эффективности лечения: значительно снижается количество ОРВИ с 10–18 в году до 2–3 в году, сокращается число бактериальных осложнений в 4–6 раз, ускоряется выход в клиническую ремиссию в 6–8 раз, длительность ремиссии увеличивается в 8–10 раз, с 7–10 дней до 100–150 дней, повышается качество жизни детей. Положительные клинические эффекты сопровождаются позитивной динамикой со стороны системы ИФН и иммунной системы.
Таким образом, дети из группы ЧДБ, страдающие повторными («упорно-рецидивирующими») ОРВИ, упорно-рецидивирующими вирусно-бактериальными инфекциями респираторного тракта и ЛОР-органов, в ряде случаев иммунокомпрометированы — имеют серьезные нарушения в иммунной системе по типу ВИД и в системе ИФН. Они нуждаются в проведении адекватной пролонгированной интерфероно- и позитивной направленной иммунотерапии, которые должны органично включаться в программы иммунореабилитации и сопровождаться обязательным мониторированием иммунного статуса и системы ИФН. Описанная выше тактика интерфероно- и иммунотерапии позволяет достигать положительных клинико-иммунологических эффектов: более легкого течения заболеваний в остром периоде, сокращения периода острых проявлений, значительного удлинения периода ремиссии, уменьшения количества бактериальных осложнений на фоне восстановления функционирования иммунной системы и системы ИФН.
И. В. Нестерова, доктор медицинских наук, профессор
Учебно-научный медицинский центр Управления делами Президента РФ, Москва
Таблица
Дефекты противовирусного иммунитета у ЧДБ детей (частота встречаемости в %)


