Ретролентальная фиброплазия у новорожденных что это
РЕТРОЛЕНТАЛЬНАЯ ФИБРОПЛАЗИЯ
РЕТРОЛЕНТАЛЬНАЯ ФИБРОПЛАЗИЯ (лат. retro назад, сзади + lens, lentis чечевица, здесь — хрусталик; лат. fibra волокно + греч. plasis формирование; син. ретинопатия недоношенных) — двустороннее заболевание глаз, при к-ром за хрусталиком образуется плотная соединительнотканная мембрана, спаянная с отслоенной сетчаткой.
Развивается преимущественно у недоношенных детей (см.), родившихся с весом (массой) менее 1600 г и дыхательными нарушениями. Впервые заболевание описано в 1942 г. Терри (Т. L. Terry).
Основной причиной Р. ф. является патогенное действие избыточного количества кислорода при содержании недоношенных в кислородных палатах. Высказано мнение о возможности возникновения у ребенка после рождения относительной гипероксии в тех случаях, когда наблюдалась внутриутробная гипоксия.
В течении Р. ф. различают 5 стадий. В первой стадии отмечается расширение и извитость периферических сосудов сетчатки, во второй — неоваскуляризация сетчатки, пролиферация соединительной ткани по ходу ее сосудов, третья стадия характеризуется кровоизлияниями в сетчатку и стекловидное тело, врастанием новообразованных сосудов и распространением пролиферативного процесса в стекловидное тело. При первой и второй стадиях может наступить спонтанная регрессия процесса, выражающаяся в запустевании новообразованных сосудов сетчатки. Чаще заболевание прогрессирует и переходит в четвертую стадию, когда в результате образования соединительнотканных тяжей и шварт в стекловидном теле наступает частичная отслойка сетчатки (см.), идущая от диска зрительного нерва. В дальнейшем, в пятой стадии, сетчатка отслаивается полностью и вместе с соединительной тканью образует за хрусталиком плотную, серого цвета мембрану различной толщины. Фиброз стекловидного тела может быть тотальным. Зрение понижается до слепоты. Изменения глаз при Р. ф. претерпевают полный цикл развития в течение 4—6 мес. В последующем может задерживаться нормальный рост глаза (см.), нередко развивается иридоциклит (см.), катаракта (см.), вторичная глаукома (см.).
Лечение Р. ф. неэффективно. Прогноз при прогрессировании процесса тяжелый.
Профилактика — правильное дозирование кислорода недоношенным детям (см. Кислородная терапия), антенатальная охрана плода (см.).
Библиография: Кацнельсон А. Б. Аномалии развития и заболевания глаз в раннем детском возрасте, JI., 1957, библиогр.; Barr С. С., Rice Т. А. а. Michels R. G. Angioma-like mass in a patient with retrolental fibroplasia, Amer. J. Ophthal., v. 89, p. 647, 1980; Fledelius H. Prematurity and the eye, Acta ophthal. (Kbh.), v. 128, suppl., p. 159, 1976; Kingham J. D. Acute retrolental fibroplasia, Arch. Ophthal., v. 95, p. 39, 1977; Terry T. L. Extreme prematurity and fibroblastic overgrowth of persistent vascular sheath behind each crystalline lens, Amer. J. Ophthal., v. 25, p. 203, 1942.
Ретролентальная фиброплазия у новорожденных что это
Ретинопатия недоношенных (PH) впервые описана Terry. Это состояние, затем известное как ретролентальная фиброплазия, является заболеванием недоразвитых сосудов сетчатки. Оно было крайне редким до 1940-х годов. Ретинопатия развивается после осмотра нормального глазного дна при рождении. Клинически и экспериментально доказано потенциальное токсическое влияние кислорода на недоразвитые сосуды сетчатки, что приводит к сокращению использования кислорода у недоношенных новорожденных. Это приводит к резкому уменьшению частоты ретинопатии недоношенных (PH), но, хотя кислород играет центральную роль, существует множество других факторов, вносящих свой вклад в патогенез, которые были всесторонне рассмотрены.
а) Развитие сосудов сетчатки. Сосудистая сеть сетчатки развивается для обеспечения метаболических потребностей сетчатки за исключением области фовеа, где она имеет другую конфигурацию. В начале развития сетчатка получает все питательные вещества из хориоидеи, сосуды в которой формируются примерно с шестой недели гестации; васкуляризация сетчатки начинается на 14-15 неделе гестации. Клетки эндотелия сосудов, микроглия, перициты и астроциты мигрируют центробежно от диска зрительного нерва, пролиферируют и выстраиваются в сосудистые столбики, в которых формируется просвет и происходит дифференциация в капилляры. Капилляры перестраиваются и формируют зрелую сосудистую сеть с зонами, свободными от капилляров. Ткань сетчатки в ответ на избыточность или недостаточность кислорода путем сокращения или стимулирования роста микрососудов подстраивается под метаболические потребности сетчатки.
Кислород зависимый фактор роста эндотелия сосудов (VEGF) играет роль на всех стадиях развития сосудов; остальные факторы также участвуют в этом процессе. Один из кислород-независимых инсулиноподобных факторов роста (IGF-1), который контролирует активацию VEGF по Akt-сигнальному пути, регулирует жизнеспособность клеток эндотелия; низкие значения фактора приводят к снижению продолжительности жизни и росту эндотелиальных клеток сосудов.
Васкуляризация назальной части сетчатки происходит к 32 неделе гестации, височной — сразу после этого. Сосуды сетчатки у недоношенных новорожденных вытянуты, относительно прямые и сужаются в концах по направлению к серой аваскулярной периферии. Область фовеа офтальмоскопически дифференцируется около 40 недели.
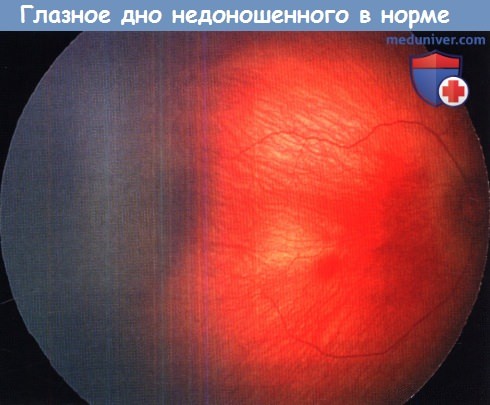
Обращает внимание вытянутость и небольшой калибр сосудов сетчатки—артериолы едва различимы. Сосуды сужаются по направлению к серой аваскулярной периферии.
Макулярная область дифференцируется плохо. Это и многие другие изображения были получены при помощи широкоугольной цифровой камеры.
б) Патогенез ретинопатии недоношенных (РН). Ограничение кислорода не позволяет избежать развития ретинопатии недоношенных (РН); полагаем это будет «казаться наивным в свете современного понимания». В настоящее время ретинопатия недоношенных (РН) является излечимым, но не предотвращаемым заболеванием. Согласно первой — «классической» теории, ретинопатия недоношенных (РН) состоит из двух равнозначных фаз:
1. Гипероксическая фаза приводит к сужению артериол сетчатки.
2. Облитерация сосудов с гибелью эндотелиальных клеток капилляров сетчатки в ответ на исчезновение гипероксической среды.
Вторая теория — «щелевидное соединение» — основана на активности мезенхимальных веретенообразных клеток-предшественников капилляров сетчатки. Мезенхимальные веретенообразные клетки мигрируют центробежно от диска зрительного нерва и образуют капилляры сразу же за линией их перемещения. В относительно гипоксическом внематочном состоянии между соединяющимися веретенообразными клетками образуются плотные связи или щелевидные соединения, мешающие нормальной миграции клеток и формированию сосудов. Ангиогенные факторы, секретируемые щелевидно соединенными веретенообразными клетками, стимулируют процессы неоваскуляризации.
Современная концепция патогенеза ретинопатии недоношенных (РН) включает как классическую теорию, так и теорию щелевидных соединений. VEGF секретируется в ответ на физиологическую гипоксию зрелой аваскулярной сетчатки. Гипоксия вызывает остановку роста сосудов и апоптоз части сосудов сетчатки и регресс капилляров с последующей стимуляцией VEGF вследствие ишемии сетчатки.
Это приводит к неоваскуляризации, известной как ретинопатия недоношенных (РН).
Выделяют две фазы VEGF-А:
1. Сосудоподдерживающая роль, уменьшающаяся вследствие гипоксии, приводит к деактивации (снижению) VEGF-А с прекращением роста сосудов и регрессом капилляров.
2. Вследствие гипоксии последующая избыточная активация VEGF-А с вазопролиферацией, известной как ретинопатия недоношенных (РН).
В сетчатке мышей выявлены два типа рецепторов к VEGF-A: VEGFR-1, обеспечивающих продолжительность существования сосудов сетчатки (фаза 1), и VEGFR-2 обеспечивающих проницаемость эндотелия и вазопролиферацию.
IGF-1 — соматический фактор роста, контролирующий активацию VEGF: когда IGF-1 недостаточно, сосуды не растут. Уровни плацентарного IGF-1 повышаются на втором и третьем семестрах и снижаются сразу после преждевременного рождения. Кислородонезависимый IGF-1 и кислородозависимый VEGF— синергистьци IGF-1 позволяет максимально функционировать VEGF при низких значениях. Медленное восстановление «нормального» уровня сывороточного IGF-1 может прогнозировать вторую фазу пролиферативной PH; причина этого не установлена, но ее связывают с рядом стимулирующих методов лечения.
Классическая теория и теория щелевидных соединений сходы с теорией VEGF. Все они основаны на задержке нормального васкулогенеза и оксидативном повреждении. Таким образом, гипоксия первично важна и остановка роста сосудов вследствие деактивации VEGF не оказывает прямого цитотоксического эффекта на сосуды сетчатки. Не все из ранних теорий патогенеза PH могут быть включены в современную концепцию: выделение фаз «кислорода» и «комнатного воздуха» не могут быть применены в современной модели.
в) Факторы риска ретинопатии недоношенных (РН) или ассоциированные состояния. Главным фактором риска развития PH является уровень недоношенности, выражающийся в массе тела при рождении или гестационном возрасте, первый из них является более значимым показателем.
Клинические исследования подтвердили связь оксигенации и PH, а также уровня транскутанного парциального давления кислорода (РО2) более 80 мм рт.ст., его влияние и значение. Уровень кислорода особенно критичен для развития PH в течение первых нескольких недель поcле рождения. Безопасные уровни применяемого кислорода в клинической практике до сих пор не установлены.
Ретинопатия недоношенных (PH) может развиваться у младенцев, которые никогда не получали кислород и у недоношенных с врожденным пороком сердца с первичным цианозом (синего типа). Предполагается связь между неонатальной гипоксией и PH. Такая возможная связь PH с гипероксией и гипоксией не настолько противоречива. Относительная гипероксия через VEGF может приводить к первичному повреждению капилляров сетчатки; последующая ишемия стимулирует гиперпродукцию VEGF и вазопролиферацию, объясняя связь возвратного апноэ и церебральной ишемии, происходящей при PH.
Исследование STOP-ROP изучило эффективность и риски вспомогательной оксигенотерапии для предпороговой болезни, но не показало положительного эффекта. Метаанализ показал, что «поздний» (> 32 недели постменструального возраста ребенка — ПВМ) высокий уровень кислорода связан с уменьшением вероятности тяжелой PH. Кислород по-прежнему играет центральную роль при PH. Дети с целевым уровнем оксигенации 94-98% имели большую вероятность развития PH, требующего лечения, по сравнению с целевым уровнем оксигенации 70-90%, без повышения уровня заболеваемости болезнями нервной системы в будущем.
Несмотря на более высокие уровни кислорода, в рандомизированном контролируемом исследовании разницы в развитии младенцев, неврологическом статусе или степени PH при уровнях сатурации кислорода 91-94% и 95-98% выявлено не было. Риск развития PH не следует рассматривать в отрыве от общего состояния ребенка. Более низкий уровень кислорода снижает частоту слепоты из-за PH, но за счет снижения продолжительности жизни и более высокой заболеваемости.
В отличие от гиперкапнии ацидоз является фактором риска развития PH. Высокие значения pCO2, РаО2 и низкий pH в первые три дня после рождения связаны с тяжелой РН и гипергликемией — фактором риска, возможно связанным с инсулинорезистентностью. Дородовое применение стероидов может обладать протективным свойством для РН, но не при их применении после родов.
Не выявлено разницы в частоте развития РН у младенцев латиноамериканцев и белых нелатиноамериканских младенцев, тогда как индопакистанцы более предрасположены к развитию РН, чем европейские народы. Младенцы афрокарибского происхождения более или менее предрасположены к РН. Существует большое сходство развития РН у монозиготных близнецов. Все мутации, связанные с РН, затрагивают Wnt-сигнальный путь, который также окружает гены Норри и семейной экссудативной витреоретинопатии; значение этого пока не ясно. Многоплодные роды, по сути, не повышают риск РН, но у идентичных близнецов она протекает сходным образом. У неидентичных близнецов у более младшего ребенка риск РН выше. Мужской пол является фактором риска как и вспомогательные репродуктивные технологии, последние, по-видимому, связаны с многоплодными родами.
Выявлен низкий уровень антиоксиданта витамина Е у недоношенных новорожденных; прием пищевых добавок с самого начала не снижает частоту РН, но уменьшает ее тяжесть. Из-за побочных эффектов витамина Е его профилактическое применение не рекомендуется, хотя Raju и соавт. в мета-анализе профилактического применения витамина Е сообщили о снижении вероятности стадии 3+ РН и предложили провести переоценку его применения. Анемия часто встречается у недоношенных младенцев; им может переливаться гемоглобин взрослых, который хуже связывает кислород, по сравнению с фетальным гемоглобином, таким образом к тканям поступает больше кислорода, вызывая гипероксию, теоретически повышая риск РН. Это предполагает связь РН и переливания крови, но не подтверждает ее. Рекомбинантный эритропоэтин — цитокин, регулирующий фетальный эритропоэз и играющий важную роль в ангиогенезе, может в настоящее время применяться в лечении неонатальной анемии. Его роль в РН еще не ясна, включая и сроки.
Сурфактант снижает смертность, тяжесть респираторного дистресс-синдрома и хронических заболеваний легких у очень недоношенных новорожденных, но его влияние в отношении РН менее ясно.
Ранее фактором риска предполагалось воздействие света. В исследованиях Нерпег с соавт., Locke и Reese не приведено достаточных доказательств; более поздние исследования не подтвердили этого, в то время как вспомогательный кислород мог подавлять любое воздействие света. Свет за счет повреждения ткани сетчатки может вызывать выработку свободных радикалов и вызывать РН. Уменьшение освещенности у новорожденных снижало вероятность и тяжесть РН, но это не было подтверждено исследованием LIGHT-ROP и другими исследованиями.
Антенатальная инфекция и воспаление не связаны с развитием РН у индивидуума, но в совокупности они могут повышать риск тяжелой РН; послеродовая системная грибковая инфекция является фактором риска, как для развития, так и тяжести РН.
Многие факторы активны одновременно и неодинаково в зависимости от стандартов оказания неонатальной помощи. Таким образом, характеристики детей с развивающейся РН в некоторых странах отличаются от детей в других странах: крупные и более зрелые новорожденные находятся в большем риске в менее развитых странах, где необходимо учитывать неограниченное использование кислорода и развитие сепсиса.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Ретинопатия недоношенных (Ретролентальная фиброплазия)
Подробнее о диагнозе
Что такое ретинопатия недоношенных (Ретролентальная фиброплазия)
Ретинопатия недоношенных: обратите внимание на извитость сосудов сетчатки.
Ретинопатия недоношенных, также известная как ретролентальная фиброплазия, это серьезное заболевание, поражающее сетчатку недоношенных детей. Она связана с широким использованием большой концентрации кислорода для обеспечения дыхания преждевременно родившихся малышей. В этом смысле, ретинопатия недоношенных — это следствие все большего вторжения человека в природные процессы. В прошлом дети, родившиеся на ранних сроках беременности, просто не выживали. В настоящее время современный уход и системы поддержания жизнедеятельности позволяют сохранять жизнь 500-граммовым плодам, родившимся за 3 месяца раньше положенного срока. Условия развития в атмосферном воздухе и при естественном освещении резко отличаются от абсолютной темноты полости матки, где плоду кислород доставляется с кровью матери. Именно эти факторы объясняют развитие ретролентальной фиброплазии.
Здесь нужно отметить, что в каждой стране пик заболевания ретинопатией недоношенных приходится на разные годы, что прежде всего определяется уровнем общего социально- экономического развития того или иного государства. В США большое число заболевших пришлось на 50-е годы, когда было введено применение газа с высоким содержанием кислорода для дыхания недоношенных. В современных условиях, хотя и были сделаны соотвествующие выводы, в развитых странах заболеваемость еще остается на достаточно высоком уровне, чтобы с ним мириться, поскольку выживаемость недоношенных с очень низким весом растет. До развивающихся стран неонатальные технологии пришли относительно недавно, что вкупе с высокой рождаемостью в этих странах делает проблему ретинопатии недоношенных колоссальной.
Итак, факторы риска для заболевания ретинопатией недоношенных — это низкий вес при рождении (менее 1,4 кг) и преждевременные роды (26–28 недель).
У недоношенных нормальное развитие и рост сосудов сетчатки может останавиться, и тогда начинают развиваться патологические сосуды. Проблема с патологическим ростом сосудов, известным как неоваскуляризация, заключается в том, что эти сосуды не выполняют своей функции по доставке кислорода к сетчатке. Более того, новообразованные сосуды приводят к большому количеству вторичных осложнений.
Ретинопатия недоношенных подразделяется на 5 стадий в зависимости от тяжести заболевания. Прогрессирование заболевания к последним стадиям может привести к образованию рубцовой ткани в сетчатке и стекловидном теле, что ведет к развитию отслойки сетчатки, кровотечению в полость стекловидного тела (гемофтальму), косоглазию и амблиопии. У многих детей с ретинопатией недоношенных развивается близорукость.
Признаки (симптомы) ретинопатии недоношенных
Поскольку новорожденные не могут рассказать своих жалоб, неонатологи, педиатры и офтальмологи обращают внимание на следующие факторы риска развития ретинопатии недоношенных:
Родители детей с ретинопатией недоношенных до 2-летнего возраста должны обращать внимание на появление следующих сигнальных симптомов:
Диагностика ретинопатии недоношенных
Малыши с высоким риском ретинопатии недоношенных должны пройти офтальмологическое обследование на 4 — 6 неделе жизни. После расширения зрачков закапыванием капель доктор проводит осмотр глазного дна при помощи офтальмоскопа. Во время обследования ребенок находится на руках у родителя.
Независимо от того, требуется лечение или нет, эти дети должны проходить повторные осмотры с рекомендуемым интервалом, чтобы убедиться, что развитие болезни остановилось, или появилась необходимость в лечении.
Лечение ретинопатии недоношенных
У некоторых детей с первой — второй стадией болезни улучшение происходит без лечения. В других случаях необходимо начать лечение, если заболевание достигло порогового уровня. Этот термин означает наличие третьей стадии ретинопатии недоношенных.
Для предупреждения разрастания новообразованных сосудов, периферические области сетчатки могут быть заморожены при криоретинопексии. Как альтернатива, с этой же целью может быть использован лазер — лазерная коагуляция сетчатки. Оба вида лечения оставляют постоянные рубцы на периферии сетчатки, но часто они справляются со своей задачей — сохранением центрального зрения.
В наших условиях, к сожалению, довольно часто на проблемы ребенка со зрением обращают внимание очень поздно, когда заболевание находится на четвертой — пятой стадии. В такой ситуации очень мало можно сделать, чтобы вернуть ребенку зрение. Если родители спохватываются до того, как ребенок пойдет в школу, можно надеяться, что удаление рубцов из стекловидного тела приведет к прилеганию сетчатки, а лечение амблиопии окажется успешным. В таком случае шансы на функционально значимое зрение остаются. Понятно, что прогноз на зрение у всех индивидуален.
Материалы о витреоретинальной хирургии, заболеваниях сетчатки и методах их лечения
Рождение ребенка – всегда счастье для женщины. Однако для некоторых оно омрачается проблемами, связанными со здоровьем новорожденного малыша. В некоторой степени этому способствует прогресс в области медицины, позволяющей выжить младенцам, у которых, казалось бы, уже нет шансов.
Почему развивается болезнь
Основная причина фиброплазии – воздействие кислорода в больших концентрациях на недоношенных младенцев, находящихся в кювезах. Кислород вместе с воздухом подается в таких количествах для обеспечения дыхания.
Раньше медицина не могла обеспечить выживание младенцев, родившихся пятимесячными, с массой тела 500 граммов. Сейчас достижения современной науки и методики выхаживания позволяют таким деткам расти и развиваться. Однако побочным результатом этого, к сожалению, нередко является развитие ретинопатий с неминуемой потерей зрения.
Почему развитие фиброплазии нередко встречается у недоношенных? Это происходит потому, что организм преждевременно рожденного младенца еще не готов к воздействию атмосферного воздуха и условий освещения. Еще совсем недавно он находился в «водной среде» матки в абсолютной темноте, а кислород в нужных концентрациях доставлялся с кровью через плаценту. В инкубаторе для поддержания жизненных функций на него «воздействуют» воздухом, насыщенным кислородом.
Этот элемент вызывает сужение капилляров сетчатки и гибель ее эндотелиальных клеток. Ответной реакцией на «разрушения» является разрастание патологической сосудистой сети и соединительной ткани.
Какие дети входят в группу риска
Младенцы с такой патологией поначалу ничем не отличаются от других (за исключением, конечно, признаков недоношенности). Они не могут пожаловаться и даже не всегда возвещают криком о своем состоянии. Как правило, родители не сразу замечают у своего чада нарушения в зрительном восприятии. Проблема вскрывается, когда ребенок начинает реагировать на окружающие предметы.
К факторам риска относятся:
вес при рождении ниже 1400 граммов;
нестабильность состояния младенца.
На заметку. Существует предположение, что фиброплазия может явиться следствием гипоксии у ребенка, рожденного в срок. Она развивается в результате перенасыщения кислородом тканей при переходе из условий с его недостатком.
Стадии развития болезни
В процессе течения заболевания определено пять стадий. Первая и вторая из них считаются функциональными, после них может произойти обратное развитие, однако чаще всего процесс имеет склонность к прогрессированию.
первая: сосуды сетчатки расширяются и становятся извитыми;
вторая: дальнейшее разрастание сосудистой сети, ее прорастание соединительнотканными волокнами;
третья: прорастание соединительной ткани в стекловидное тело, кровоизлияния в него и сетчатку;
четвертая: образование рубцов и шварт в сетчатке и стекловидном теле, отслойка сетчатки;
образование плотной мембраны за хрусталиком, стекловидное тело при этом может полностью фиброзироваться.
Симптомы болезни
Если ребенок принадлежит к группе риска по фиброплазии, родители с момента рождения должны обращать внимание на развитие малыша в процессе взросления. Их должно насторожить, что малыш слишком близко держит игрушки к глазам, пытаясь рассмотреть их. Когда ему предлагают что-либо, не замечает мелкий предмет на расстоянии.
В редких случаях малыш может обладать односторонним зрением, при этом чаще будет моргать одним глазом. Данная патология иногда сопровождается косоглазием.
На заключительных стадиях болезни, если внимательно присмотреться, можно определить легкое беловатое помутнение в области зрачка. Необратимые изменения приводят к торможению роста глазного яблока, при этом становится заметно, что глаза выглядят намного меньше, чем должны быть.
Диагностика
Младенцы с риском развития патологии должны наблюдаться у офтальмолога и регулярно проходить осмотры, начиная с 4-6-недельного возраста.
Основным методом диагностики является офтальмоскопия. Врач видит измененные сосуды сетчатки, ее перерождение в соединительнотканные структуры, кровоизлияния.
Применяется обследование глаза с использованием специальной аппаратуры: биомикроскопия, эхография.
Лечение и прогноз
Первая и вторая стадии заболевания могут закончиться обратным развитием, и ребенок обойдется без лечения. Однако, к сожалению, такое происходит нечасто. Процесс прогрессирует, переходя в следующую стадию.
Чем раньше замечена патология и начато лечение, тем выше шансы, что малыш будет видеть. В основном применяются хирургические методы.
Чтобы предупредить разрастание патологических сосудов сетчатки, производится криоретинопексия, они подвергаются заморозке. В других случаях проводят лазерную коагуляцию. И тот, и другой метод вмешательств сопровождается образованием рубцов на периферии сетчатки. Однако центральное зрение при этом сохраняется.
Исход заболевания индивидуален и во многом зависит от площади поражения и своевременности лечебных мероприятий. Многим детям после операции сохраняется зрение, хотя и не полностью. В большинстве случаев терапия направлена на предупреждение развития глаукомы, катаракты, различных иридоциклитов, которые нередко сопутствуют этой болезни. В запущенном состоянии эти патологии в сочетании с фиброплазией могут привести к потере глаза.
Заключение. Как можно раньше заметить болезнь и избежать плачевных последствий
Ребенок – это радость для родителей. Но если он родился недоношенным или с какой-либо другой патологией, к нему нужно особое внимание и должный уход. При малейшем подозрении на отклонения в поведении и развитии мама или папа должны сообщить педиатру. Конечно, такой малыш регулярно должен обследоваться у детского офтальмолога. При соблюдении всех правил вы сможете вовремя выявить болезнь, избежать прогрессирования и сохранить малышу зрение.
