Рпэ простаты что это
Рак предстательной железы: почему возникает, симптоматика, методы диагностики и лечения
Введение
Согласно данным множества исследований, отмечается неуклонный рост случаев обнаружения первичного рака предстательной железы (РПЖ). В России это заболевание находится на 4-м месте среди всей онкологии, выявляемой во время профосмотров. Опережает его рак шейки матки, молочной железы и губы. В западных странах рак простаты составляет 25% от всех онкологических заболеваний.
Что такое рак простаты?
РПЖ представляет собой злокачественное новообразование, которое развивается из тканей предстательной железы.
Предстательная железа, или простата, – мужской репродуктивный орган, по размерам схожий с каштаном. Он находится под мочевым пузырем и охватывает передний отдел мочеиспускательного канала.
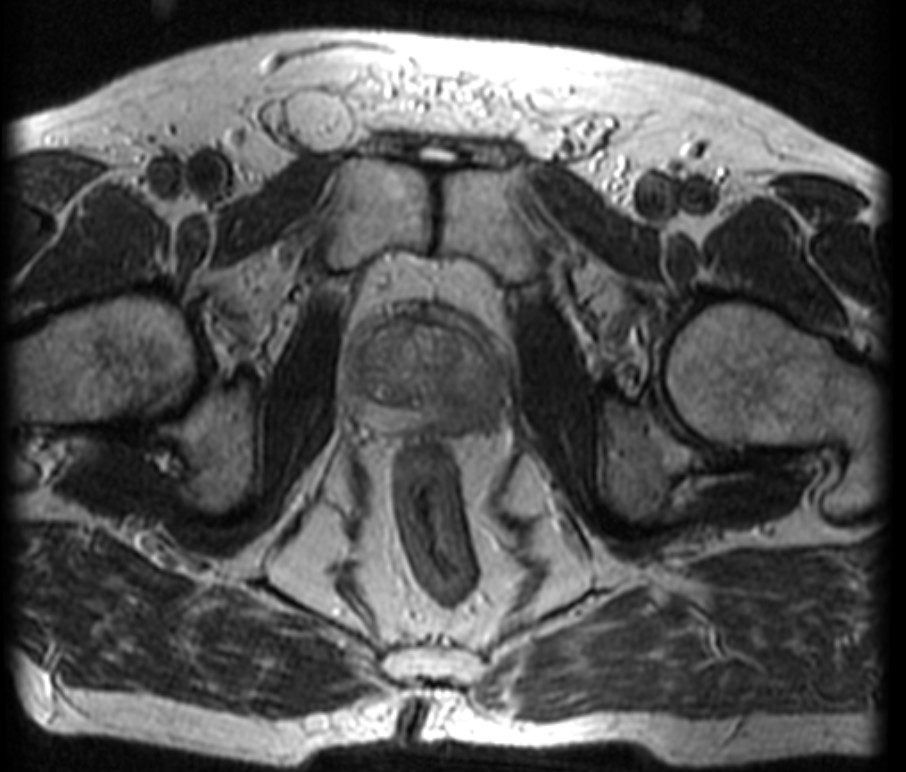
Рис. 1. МРТ (Т2-взвешенные изображения) картина поражения левой доли предстательной железы.
Разновидности рака предстательной железы
В 95% случаев РПЖ развивается из эпителиальных клеток собственных желез (их называют «ацинусы»), из которых сформирована периферическая часть предстательной железы. Эта форма болезни называется «ацинарная аденокарцинома». В остальных 5% случаев диагностируется интрдуктальная разновидность, для которой характерно более агрессивное течение.
Важная характеристика аденокарциномы – степень ее дифференцировки, которая выявляется при гистологическом исследовании биоптата или биоматериала, полученного в ходе операции. Дифференцировка сегодня выражается шкалой Глисона (Gleason), в соответствии с которой присваивается сумма баллов: от 6 (самый благоприятный прогноз) до 10 (самый неблагоприятный вариант).
Характерные признаки заболевания
Риск развития РПЖ растет с возрастом: средний показатель в этой категории заболевших – 68 лет. Существуют также факторы риска, то есть то, что повышает шанс появления онкологического заболевания. Современной медициной не выявлены достоверные факторы, которые приводят к повышению риска развития РПЖ (какие-либо препараты, характер рациона, вредные привычки, плохая экология и др.). Поэтому основным фактором остается возраста, а также возрастной гормональный дисбаланс (между эстрогенами и андрогенами).
Симптоматика, первые признаки
На ранних стадиях злокачественная опухоль обычно не проявляет себя. Кроме аденокарциномы, у людей с повышенным риском развития РПЖ почти всегда присутствуют сопутствующие патологии (простатит, аденома простаты), и они могут давать симптоматику. Чаще всего встречаются следующие симптомы:
Таким образом, чем выше стадия, тем больше вероятность проявления симптоматики. Чаще всего РПЖ обнаруживается во время профилактического обследования (оно рекомендовано всем мужчинам старше 40-ка лет). Такое обследование включает в себя:
ПСА – это маркер, используемый для раннего выявления РПЖ. Он достаточно чувствителен и специфичен, чтобы заподозрить наличие рака на начальной стадии. Кроме ПСА, анализу могут подвергаться его производные – индекс здоровья простаты, плотность ПСА, соотношение свободного ПСА и общего.
Методы диагностики
Основа диагностики РПЖ – биопсия предстательной железы, иными словами, морфологическая верификация.
Показания к биопсии:
Важно! Если уровень ПСА ниже верхней допустимой границы, это не всегда говорит о том, что РПЖ отсутствует. Примерно 25% случаев заболеваемости отмечаются на фоне нормальных значений этого показателя. Поэтому решение о необходимости проведения биопсии должно приниматься после комплексного обследования, которое включает все виды диагностики.
Варианты биопсии простаты:
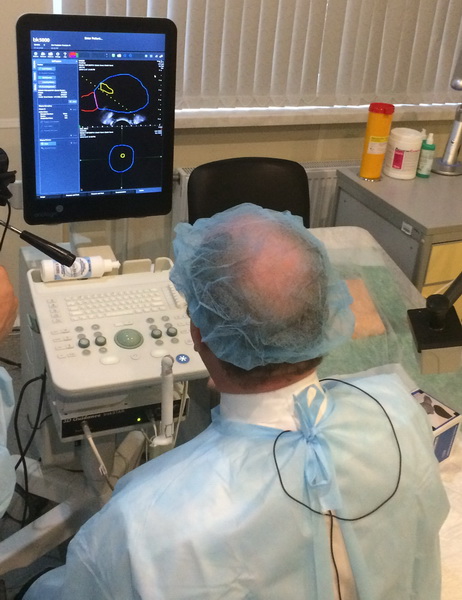
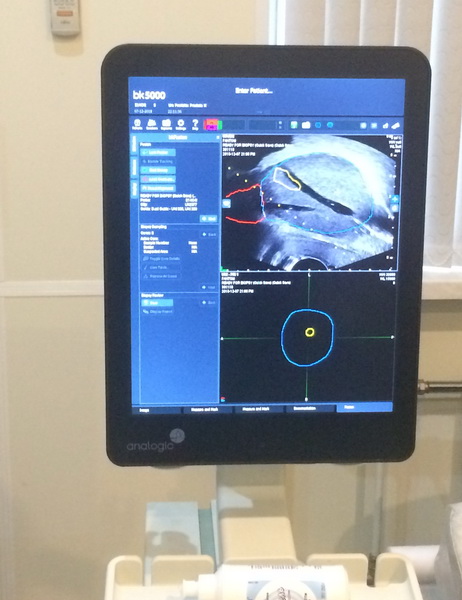
Рис. 2 А., 2 Б. Фьюжн-биопсия. Мастер-класс в НМИЦ онкологии им. Н.Н. Петрова
Стадии рака предстательной железы
Стадирование РПЖ и определение группы риска рецидивирования после возможной терапии производятся после гистологической верификации заболевания.
Стадирование при стандартном подходе подразумевает остеосцинтиграфию и МРТ органов малого таза. Магнитно-резонансная томография нужна, чтобы выявить степень локального распространения процесса в зоне простаты (прорастание в семенные пузырьки, выход новообразования за капсулу железы), а также определить, есть ли поражение регионарных лимфоузлов.
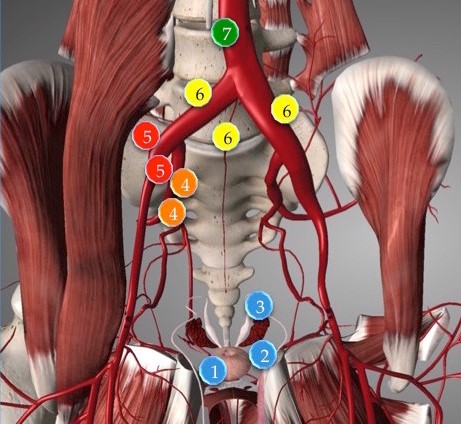
Рис. 3. Пути распространения рака предстательной железы в лимфоузлы таза.
В случае необходимости дополнительно проводится КТ органов груди или брюшной полости.
Цель проведения остеосцинтиграфии – выявление возможного поражения опухолью костей скелета.
Могут назначиться дополнительные исследования – рентгенография (прицельная), УЗИ, урофлоуметрия.
Группа риска определяется, исходя из уровня ПСА на момент до начала терапии, суммы Глисона, согласно данным биопсии, и клинической стадии болезни. Группа риска может быть низкой, промежуточной и высокой. Ее определение крайне важно, чтобы выбрать оптимальный метод лечения.
ПСА от 10 до 20 нг/мл
Методики лечения
В соответствии с результатами многоцентрового проспективного рандомизированного исследования ProtecT (2016) лучевая терапия и хирургическое лечения демонстрируют раную противоопухолевую эффективность и обеспечивают надежный контроль над заболеванием у большинства (более 90%) больных раком предстательной железы с низким и промежуточным риском рецидива заболевания. В настоящее время решающим фактором при выборе противоопухолевого лечения у этой категории больных является безопасность терапии и снижение риска осложнений.
Рассмотрим основные виды терапии: хирургическое лечение, брахитерапия, стереотаксическое облучение, сочетанная лучевая терапия.
Хирургическое вмешательство
РПЭ, или радикальная простатэктомия, представляет собой хирургическое вмешательство по удалению предстательной железы, а также окружающей клетчатки и лимфоузлов. При такой операции с железой единым блоком удаляют семенные пузырьки и участок канала уретры.
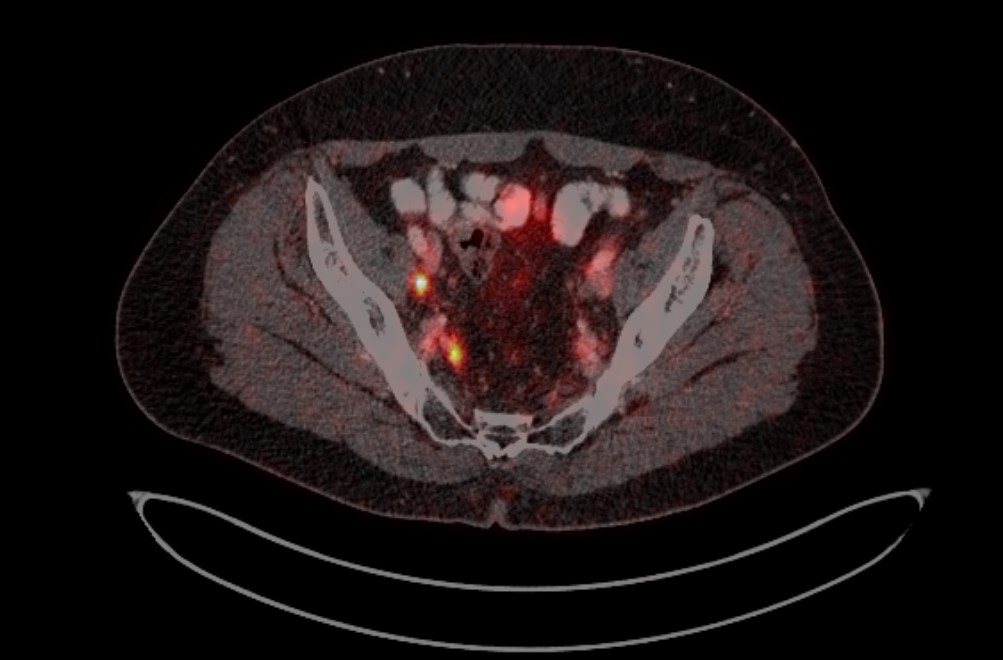
Рис. 4. ПЭТ-КТ изображения больного М. с поражением тазовых лимфоузлов
РПЭ различается по виду доступа и степени инвазивности:
Позадилонный доступ предполагает разрез в нижней части живота, через который удаляется простата и местные ткани.
Промежностная методика – это открытый способ, при котором небольшой надрез делается в зоне между анусом и кожно-мышечным мешком, то есть мошонкой. Методика позволяет удалить простату, но при ее применении нельзя также удалить неблагоприятные ткани и узлы, расположенные около железы. Если после проведения промежностной операции в органах малого таза обнаружатся раковые клетки, нужно будет дополнительно делать лимфаденэктомию. Сейчас промежностная методика применяется крайне редко.
Лапароскопическая методика – наиболее щадящая. Врач имеет доступ к пораженному органу через маленький разрез внизу живота. В него вводится камера и все нужные хирургу инструменты. Камера подает на экран изображение органов малого таза, благодаря чему врач полностью контролирует процесс, а пациент получает минимум вреда. При таком способе минимизированы кровопотери, посторонние органы почти не травмируются, эректильная функция сохраняется частично или полностью и т. д.
Рассмотрим также наиболее распространенные осложнения, которые могут возникнуть после операции на простате:
Брахитерапия
Брахитерапия представляет собой введение в ткани источников излучения. Эта методика – самая «молодая» среди способов лечения РПЖ. Сегодня это один из наиболее востребованных методов облучения простаты, обеспечивающий очень высокую избирательность подведения дозы. Основная особенность брахитерапии заключается в том, что простата облучается изнутри – источник облучения вводится непосредственно в нее. Такой метод дает возможность применять высокие дозы (100-140 Гр и более), при этом избегая высокого риска лучевого поражения не подверженных раку тканей.
Стремительный рост клинического применении брахитерапии, по сравнению с хирургическими вмешательствами, обуславливается высокой эффективностью, которая сопоставима с простатэктомией, при гораздо более низкой частоте возникновения осложнений.
Различают 2 вида брахитерапии, в зависимости от способа введения источника излучения в железу и его мощности:
При проведении низкомощностной брахитерапии в ткани простаты вживляется источник излучения и остается в них до полного распада. Долгое время при РПЖ именно этот вид брахитерапии применялся чаще всего. Наиболее часто для выполнения терапии используется изотоп радиоактивного йода, то есть I125.
Согласно многочисленным исследованиям, брахитерапия низкой мощности обеспечивает не очень высокую точность облучения. Это объясняется смещением источника излучения, изменением формы и размеров простаты, затрагиванием прилежащих здоровых органов. Ввиду этого низкомощностная методика показана в основном пациентам с самыми начальными стадиями, когда опухоль небольшая и не выходит за пределы железы. Такая брахитерапия имеет и другие существенные недостатки. Первый – это высокая частота осложнений, возникающих со стороны мочевыводящих путей, может даже возникнуть острая задержка мочи и необходимость эпицистостомы, то есть формирования надлобкового мочепузырного свища, на долгий срок. В основе осложнений – отек предстательной железы из-за того, что в ней остается несколько сотен зерен (инородных тел). Кроме того, радиоактивные зерна, если они долго находятся в организме, представляют собой источники излучения, представляющие определенную опасность для других людей. Из-за этого контакт пациента с родными ограничен (нельзя близко общаться с маленькими детьми).
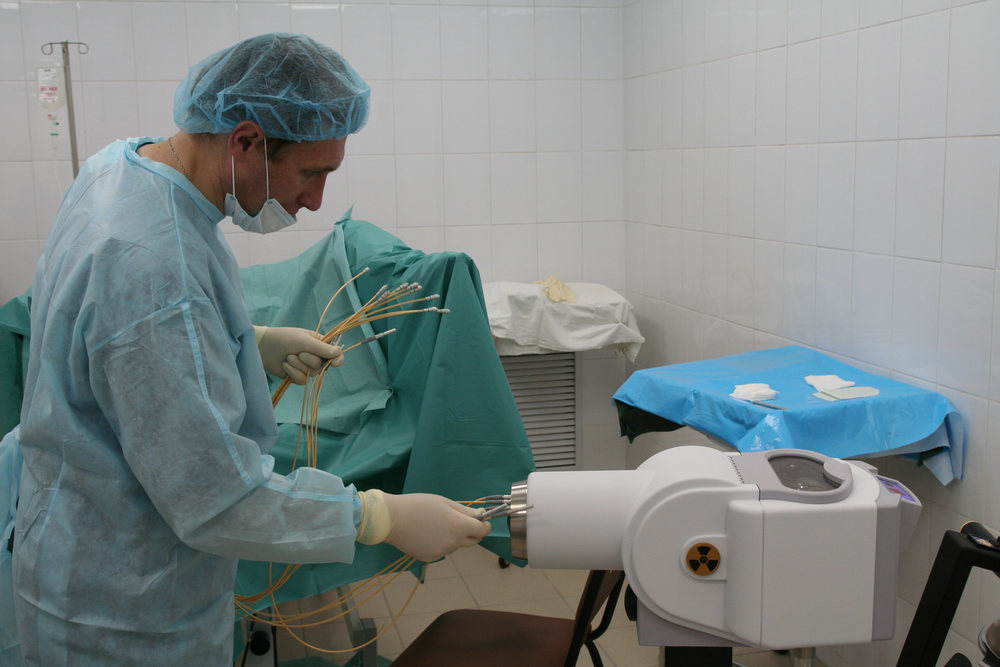
Рис. 5. Высокомощностная (высокодозная) брахитерапия
Самая современная методика внутритканевой терапии – высокомощностная брахитерапия. Источники излучения автоматически загружаются и извлекаются. Эта лучевая терапия обладает принципиальным плюсов – высокой точностью облучения, достигаемой путем введения игл под контролем специального УЗ-аппарата. Одновременно в автоматическом режиме рассчитываются дозы и возможность быстрой корректировки плана лучевого лечения. Источник излучения находится в организме пациента временно, поэтому уровень осложнений – самый низкий, по сравнению со всеми радикальными методиками терапии РПЖ, включая низкодозную разновидность брахитерапии.
Технологические особенности методики позволяют предлагать ее большинству больных, вне зависимости от размеров злокачественного новообразования и его распространенности за пределы простаты. Кроме того, высокомощностная брахитерапия – это «золотой стандарт» при комбинированном лечении, то есть одновременном использовании с дистанционным облучением у больных с неблагоприятными характеристиками новообразования.
Самый большой недостаток высокомощностной методики – высокие требования, касающиеся квалификации медицинского персонала, а также необходимость использования высокотехнологичного оборудования. Этим объясняется малая распространенность метода в России.
Противопоказания к брахитерапии подразделяются на общие и урологические. Самые частые урологические противопоказания – это серьезные нарушения процесса мочеиспускания:
Нужно отметить, что большой объем простаты, который имеет значение для низкодозной брахитерапии (50-60 см 3 ), почти не ограничивает возможности лечения в режиме высокомощностной методики.
Данные противопоказания относятся не только к брахитерапии, но и к другим методикам лучевой терапии РПЖ.
Стереотаксическое облучение
СТЛТ (стереотаксическая лучевая терапия) – высокоточная методика лечения очага РПЖ высокими дозами ионизирующего излучения.
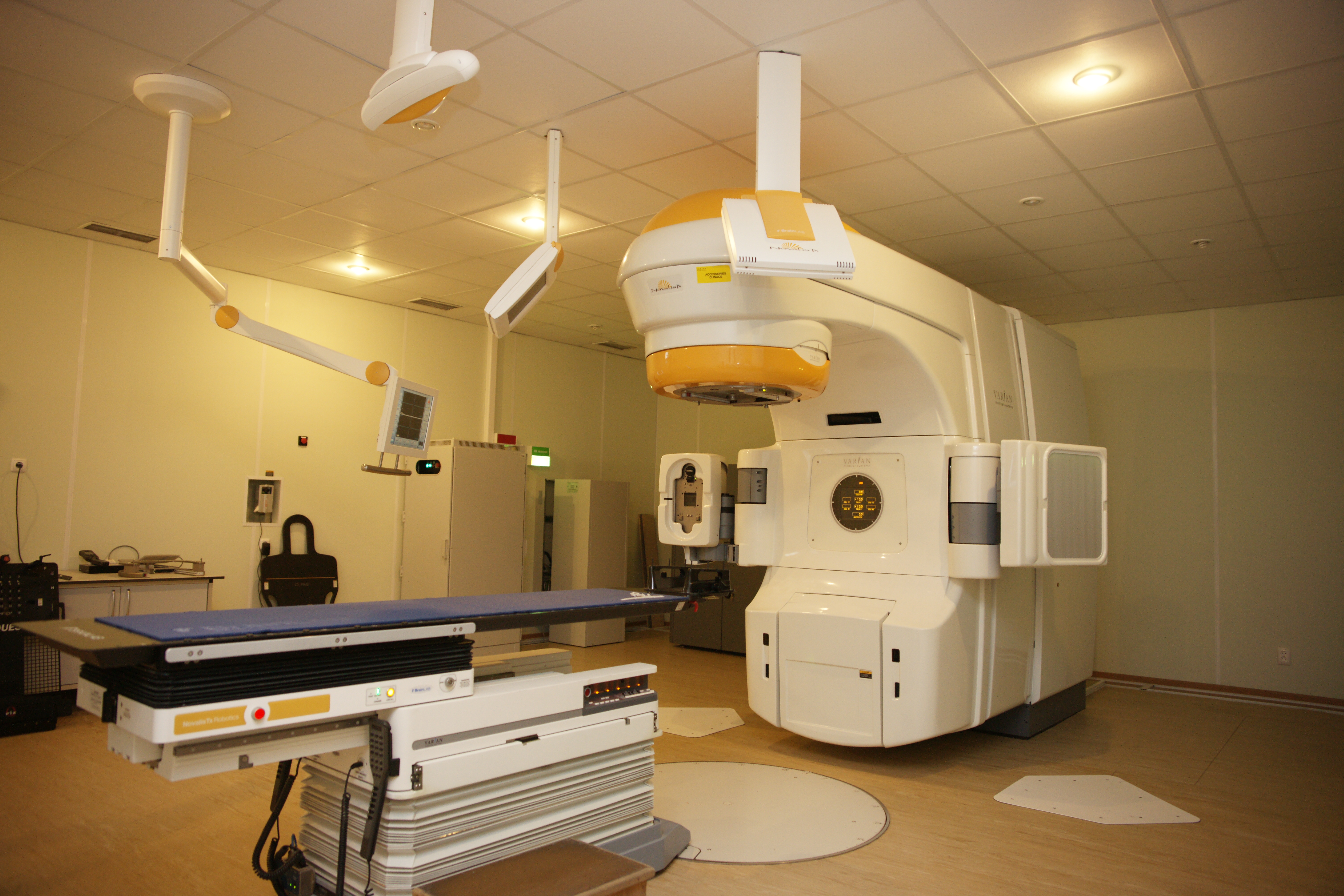
Рис. 6. Стереотаксический лучевой ускоритель
Сегодня СТЛТ при раке простаты реализуется несколькими основными методами, каждый из которых обладает своими особенностями, плюсами и минусами:
Сравнительная характеристика техник СТЛТ простаты
Радикальная простатэктомия: хирургическая операция по поводу рака простаты
Как сегодня лечится рак предстательной железы в мире?
Рак предстательной железы (РПЖ) по-прежнему является одной из самых часто встречающихся злокачественных опухолей у мужчин. В возрасте 45 — 49 лет им страдает примерно 10 — 11 мужчин из 100 000 мужского населения, в то время как в возрасте 75 — 79 лет заболеваемость составляет 1400 на 100 000 мужчин. За последние несколько десятилетий прирост заболеваемости РПЖ составлял 3% в год, что связано с увеличением продолжительности жизни мужчин и улучшением диагностики заболевания. Сегодня по распространенности и причинам смерти от онкологических заболеваний среди мужчин РПЖ находится в разных странах мира на 2 — 3 месте, уступая только раку легких и злокачественным новообразованиям пищеварительного тракта. Каждый мужчина в течение своей жизни имеет 9 — 11% шансов заболеть РПЖ и до 4,5% шансов умереть от него.
Большим достижением последних десятилетий можно считать внедрение ранней диагностики и более точного стадирования РПЖ. Анализ крови на ПСА (простатоспецифический антиген), трансректальное ультразвуковое исследование (ТРУЗИ) и мультифокальная системная биопсия простаты под ТРУЗИ-контролем позволили устанавливать диагноз РПЖ на самых ранних стадиях, когда РПЖ не выходит за пределы предстательной железы (не метастазирует). На этих ранних стадиях РПЖ может быть полностью излечен методами локального терапевтического воздействия (операция радикальной простатэктомии, наружное облучение простаты, имплантация в простату радиоактивных зерен или брахитерапия, комбинация данных методов лучевой терапии, криохирургия).
В связи с тем, что применение данных методов лечения обеспечивало выживаемость более 15 лет с момента установления диагноза РПЖ подавляющему большинству больных, они стали называться излечивающими. Если обследование показало, что опухоль простаты вышла за ее пределы и/или дала метастазы, полностью вылечится от заболевания уже невозможно. В таких случаях показано применение методов лечения, которые приостанавливают развитие РПЖ. К ним относится гормонотерапия или хирургическое (косметически щадящее удаление ткани яичек) либо медикаментозное (Золадекс, Диферелин, Касодекс, Флутамид, Флуцином, Андрокур и др.) блокирование выработки или усвоения тестостерона, мужского полового гормона, способствующего росту РПЖ. Применяются различные методы лучевой терапии и, реже, химиотерапия. Лечение РПЖ в строгом соответствии со стадией заболевания стало огромным успехом в борьбе с этим недугом. Особенно осязаема рольрадикальной простатэктомии (РПЭ), использование которой стало наиболее широким после того, когда стало возможным выявление ранних стадий РПЖ. Внедрение РПЭ и ее повсеместное применение способствовало снижению смертности от РПЖ в США на 25% за последние 10 лет (P.C. Walsh, 2002).
Как обстоит дело с диагностикой и лечением РПЖ в современной России?
В то время как в странах Западной Европы и США большую часть впервые выявленных РПЖ составляют локализованные и излечимые формы заболевания, в России по-прежнему большинство (около 70%) вновь обнаруженных РПЖ находятся уже на неизлечимой стадии. Это связано в первую очередь с пока еще низкой информированностью врачей и населения о необходимости обязательного ежегодного скрининга РПЖ для мужчин, в возрасте старше 45 — 50 лет. И хотя практически во всех крупных городах России доступен анализ крови на ПСА, далеко не все врачи, даже урологи и онкоурологи, способны правильно интерпретировать его результаты. К чему это приводит? Очень часто больного берут на операцию по поводу «аденомы» простаты, предварительно не сделав ему анализ крови на ПСА и таким образом, пропустив РПЖ. Довольно быстро после такой операции, заранее не выявленный РПЖ дает метастазы, и это приводит к гибели больного. Нередко «урологи по месту жительства» говорят пациентам, что ПСА менее 10 или даже 15 нг/мл (норма менее 4,0 нг/мл), при отсутствии опухоли, определяемой пальцем, это «ничего страшного» и можно успокоиться и не делать биопсию простаты. Такой подход приводит к тому, что заболевание переходит на неизлечимую стадию, а ведь при своевременной диагностике, пациента можно было бы вылечить.
Недавно к нам обратился мужчина 49 лет, у которого ПСА был равен 15 нг/мл. Лечащий врач об этом знал и, тем не менее, продолжал лечить больного от «простатита». Когда же мы сделали ему биопсию простаты, обнаружилось, что у пациента РПЖ высокой степени злокачественности с высокими шансами метастазирования. То, что данного пациента удастся полностью вылечить — под большим вопросом. Мы часто сталкиваемся с тем, что специалисты онкологических диспансеров лечат РПЖ не в соответствии со стадией заболевания, не так как предписывают международные стандарты, а кому как нравится и кто как умеет. Порой нам приходится видеть больных ранними и излечимыми стадиями РПЖ, которым в качестве метода выбора назначается гормонотерапия. Этого нельзя делать категорически! Ведь через 2 года после начала гормонотерапии, РПЖ очень часто становится гормоноустойчивым. Опухоль начинает быстро расти, а потом и метастазировать. Так по вине неквалифицированных врачей больные теряют свой шанс на излечение, а их близкие преждевременно теряют своих родных и любимых.
К большому сожалению, в нашей стране проблему РПЖ знают исчерпывающим образом очень немногие урологи и онкоурологи таких крупных городов России как Москва, Санкт-Петербург, Ростов-на-Дону и некоторых других. В связи с этим, уважаемые пациенты, остерегайтесь неквалифицированных рекомендаций. Постарайтесь обратиться к специалистам, имеющим специальную подготовку и знающим диагностику и лечение РПЖ в соответствии с международными требованиями и современными стандартами. По крайней мере постарайтесь получить «второе мнение» таких специалистов прежде, чем принимать решение о выборе методов диагностики и лечения РПЖ.
Кому показаны методы излечивающей локальной терапии РПЖ, и в частности операция РПЭ?
Методы излечивающей локальной терапии, включающие операцию РПЭ, наружное облучение, имплантацию радиоактивных зерен в предстательную железу и, в редких случаях, криодеструкцию (разрушение замораживанием) простаты показаны на стадиях заболевания Т1-Т3аN0M0 как самостоятельно так и в различных комбинациях. Только квалифицированный онкоуролог, обладающий исчерпывающими знаниями и достаточным практическим опытом в диагностике и лечении РПЖ, может помочь пациенту сделать правильный выбор.
Идеальным кандидатом для РПЭ является, прежде всего, пациент с подтвержденным диагнозом РПЖ на стадиях Т1-Т2а, имеющий уровень ПСА
Всегда ли надо лечить выявленную раннюю стадию РПЖ именно стандартными и общепринятыми в настоящее время методами излечивающей локальной терапии?
Конечно, любой человек боится операции. Есть психологический дискомфорт и перед лучевой терапией. К тому же многие российские урологи привыкли думать, что РПЖ лечится только гормональными препаратами, и порой дают пациентам, возможно и Вам «рекомендации» не «лезть под нож» и «полечиться таблеточками и укольчиками». Найдутся и многообразные «народные целители» и разные «альтернативные» или «нетрадиционные» практики, которые будут предлагать полечиться чем угодно: от трав, пищевых добавок и гомеопатии с иглотерапией, до питья мочи или керосина. Однако следовать таким рекомендациям чрезвычайно опасно, равно как и просто ждать и не делать ничего, думая, что ранняя стадия РПЖ медленно прогрессирует.
Один из наших пациентов с ранней стадией РПЖ, который, боясь предложенной ему операции РПЭ, пытался лечиться травами, рассказал, что когда он попросил пользовавшего его «целителя» познакомить хоть с одним вылеченным им больным, тот не смог этого сделать. Не существует ни одной опубликованной научной работы, которая бы корректно доказывала эффективность каких-либо нетрадиционных средств и методов лечения РПЖ. Зачастую ничего хорошего не сулит и простое выжидание или бездействие, а также лечение ранних стадий рака простаты без применения излечивающих методов.
Исследования естественного развития РПЖ у таких больных показали, что через 5 лет наблюдения метастазы развивались в среднем у 22 — 46% больных. Известно, что даже при наличии адекватного лечения средняя продолжительность жизни больных, у которых обнаружены метастазы РПЖ, составляет в среднем около 2-х лет. В связи с этим, если у пациента с ожидаемой продолжительностью жизни 10 — 15 лет и более выявлены ранние стадии рака предстательной железы подавляющее большинство урологов наиболее развитых стран мира рекомендуют своим пациентам оперативное лечение — РАДИКАЛЬНУЮ ПРОСТАТЭКТОМИЮ (РПЭ).
Какими преимуществами обладает РПЭ перед другими методами излечивающей локальной терапии РПЖ?
Эффективность лечения РПЖ принято оценивать по частоте рецидива заболевания (оценивается по наличию роста ПСА) и выживаемости через определенный срок после лечения (как правило, оценивают сроки выживания после лечения от 5 лет). Большинство исследований последних лет показывают, что надлежащим образом выполненная радикальная простатэктомия у правильно отобранных для этой операции больных РПЖ обеспечивает 95 — 100% выживаемость через 15 лет наблюдения и отсутствие рецидивов на этом же сроке наблюдения у 68 — 90% больных. Специалисты по лучевой терапии часто утверждают, что наружное облучение предстательной железы или имплантация в простату радиоактивных зерен дают сопоставимые результаты с операцией РПЭ. Однако, исследования, проведенные в США D’Amico A.V. и соавт. (2002) более чем на 3000 больных РПЖ показали, что это совсем не так.
По данным различных исследователей частота рецидивов РПЖ уже через 5 лет после имплантации в предстательную железу радиоактивных зерен (брахитерапия) варьирует от 12 до 45%, что значительно хуже аналогичных показателей после РПЭ. Еще чаще бывают рецидивы после криохирургии ранних стадий РПЖ.
В последние годы в ведущих странах мира появился более эффективный и безопасный метод лучевой терапии РПЖ — трехмерная конформная наружная лучевая терапия. Ряд авторов сообщает о сравнительно сопоставимой с РПЭ эффективности этого метода лечения. Однако в нашей стране подобное оборудование на момент написания данной публикации (ноябрь 2003 г.) отсутствует.
Таким образом, РПЭ обладает неоспоримым преимуществом с точки зрения эффективности по сравнению с другими методами излечивающей локальной терапии РПЖ. Это особенно ощутимо у пациентов более низкого риска (маленькая опухоль, низкая степень злокачественности) и у пациентов более молодого возраста (до 65 лет) с большей ожидаемой продолжительностью жизни. Весьма существенным фактом является то, что в России, ввиду отсутствия необходимого оборудования, а в ряде случаев достаточных квалификации и опыта лучевых терапевтов, практически невозможно провести радикальную лучевую терапию РПЖ на столь же высоком уровне, как это возможно в ведущих западных странах.
Я принял решение о выполнении РПЭ. Как подготовиться к операции, в чем заключается операция, что меня ждет в ближайшее время после операции и в дальнейшем?
Прежде всего, следует иметь ввиду, что РПЭ является одной из самых больших и сложных операций в урологии и требует к себе очень серьезного отношения как от пациента, которому она предстоит, так и от его родственников. В первую очередь следует зарезервировать около 4-х недель нерабочего времени, в течение которого происходит послеоперационная реабилитация. Особенно это относится к лицам, занимающимся физическим трудом или работой, связанной с высокой ответственностью и повышенным уровням психоэмоционального стресса.
Перед госпитализацией в стационар, пациент проходит предоперационное обследование, задачей которого является глубокое изучение общего состояния организма, оценка риска операции и наркоза. Пациенты клиники Андрос госпитализируются в стационар за 1 сутки до предстоящей операции. В день госпитализации, возможно, потребуется взять дополнительные анализы, пациент осматривается врачом анестезиологом и обсуждает с ним особенности предстоящего наркоза. Примерно около 16.00 дня накануне операции пациент начинает подготовку кишечника, который перед операцией должен быть полностью освобожден. Для этого следует прекратить употребление пищи и начать прием раствора (около 3-х литров) слабительного препарата (например Фортранс). Таким образом, в течение нескольких часов кишечник полностью очищается. В день накануне операции могут проводиться и другие мероприятия, по индивидуально установленным показаниям.
Операция радикальной простатэктомии заключается в полном удалении всей предстательной железы вместе с семенными пузырьками и прилегающими тканями. Во время операции есть несколько ключевых моментов:
После операции пациент поступает в палату интенсивной терапии, где находится до утра следующего дня. В этот период проводится восполнение кровопотери (если таковая имела место в значимом количестве), восстановление водно-электролитного баланса, проводится антибактериальная терапия с целью профилактики послеоперационных осложнений. На следующий день после операции пациента поднимают с кровати, и он начинает сидеть в кресле, ходить по палате. На второй день после операции пациент уже в сопровождении медперсонала гуляет по больничному коридору.
На 3-й день после операции, как правило, удаляются дренажи и на 4-й, 5-й дни после операции, когда у пациента восстанавливается функция кишечника, и он переводится на обычную диету, подавляющее большинство наших пациентов отправляется домой. Такое быстрое послеоперационное восстановление обеспечивается комплексом лечебно-реабилитационных мероприятий, которые были освоены специалистами клиники Андрос во время их стажировок в США и Западной Европе и успешно внедрены в нашу практику. До удаления катетера Фолея из уретры и мочевого пузыря пациент находится под тщательным амбулаторным наблюдением уролога клиники Андрос.
Как правило, 2 раза в неделю пациенты самостоятельно прибывают в амбулаторный офис клиники для различных процедур (смена повязки, контроль за состоянием катетера и мочеприемника, снятие швов и т.д.). После удаления катетера Фолея из уретры и мочевого пузыря (обычно через 3 недели после операции), пациент, как правило, восстанавливается достаточно хорошо, и некоторые даже возвращаются к работе. Через 4 — 5 недель после операции абсолютное большинство прооперированных полностью возвращаются к своей обычной жизни, за исключением интенсивных физических нагрузок, которые можно возобновить обычно через 3 месяца после операции.
Каковы наиболее частые осложнения РПЭ?
Во время операции самым грозным осложнением может стать кровотечение. Чаще всего оно имеет место у не очень опытных в данной операции хирургов, а также при условии неадекватного технического и инструментального обеспечения операции. Кровотечение более вероятно при операциях у слишком тучных пациентов, когда работать в глубокой из-за толстой жировой прослойки ране часто бывает весьма затруднительно. Высокий уровень подготовки и опыт хирурга, а также адекватное техническое и инструментальное обеспечение операции — сводят риск серьезных кровотечений при радикальных простатэктомиях к абсолютному минимуму. Если же кровотечение все-таки произошло, кровопотеря должна быть адекватно восполнена непосредственно во время и сразу после операции.
Естественно, что радикальной простатэктомии могут сопутствовать осложнения характерные для любой операции (раневая инфекция, плохое заживление раны, боли и т.д.). При качественном выполнении операции и адекватном послеоперационном ведении и, прежде всего ранней выписке из стационара, частота данных осложнений существенно снижается.
Специфическими осложнениями радикальной простатэктомии являются стойкое нарушение эрекции или эректильная дисфункция (ЭД), а также недержание мочи (НМ).
ЭД развивается из-за часто имеющего место повреждения сосудисто-нервных пучков, управляющих процессом эрекции полового члена, которые проходят по бокам в непосредственной близости от предстательной железы. Во время операции РПЭ, даже при соблюдении специальной нейросохраняющей техники, уберечь эти сосудисто-нервные пучки от частичного или полного повреждения зачастую не удается. Частота ЭД после РПЭ составляет по данным различных авторов от 15 до 80% случаев. Чем больший размер имеет опухоль в предстательной железе, тем более обширным будет оперативное вмешательство, и тем меньше шансов сохранить описанные выше сосудисто-нервные пучки. В целом большие шансы сохранить нормальную эрекцию после РПЭ имеют пациенты, имевшие хорошую эрекцию до операции. Повышает шансы сохранения эрекции комплекс ранних реабилитационных мероприятий, включающий в себя пользование препаратами, которые стимулируют эрекцию. Если все же пациент утрачивает способность совершить половой акт из-за отсутствия нормальной эрекции, ее можно восстановить как с помощью медикаментов, так и хирургическим путем.
В первые несколько недель после удаления мочевого катетера НМ в различной степени имеет место практически у всех пациентов, перенесших РПЭ. Через 6 месяцев после операции та или иная степень НМ сохраняется у 20 — 40% прооперированных, а через 1 год после операции не более чем у 10 — 12% пациентов. Чем опытнее хирург, тем меньше шансов развития НМ у прооперированного. Устранить НМ после РПЭ может помочь лечение методом биологической обратной связи (БОС), которое доступно в клинике Андрос. Если через 1 год после операции остается выраженное НМ, его возможно устранить хирургическим путем (введение формообразующего вещества под слизистую оболочку задней уретры, имплантация искусственного сфинктера мочевого пузыря, применение пластических операций — мужской уретральный слинг).
Чрезвычайно важно, чтобы врачи-урологи, которым Вы доверите выполнение операции РПЭ и Ваше послеоперационное наблюдение были способны не только выполнить саму операцию РПЭ, но и хорошо умели предупреждать, во время распознавать и полноценно лечить все осложнения, которые могут возникнуть в результате данной операции.
Как можно оценить качество жизни после РПЭ по сравнению с пациентами, получавшими другие виды излечивающей терапии ранних стадий РПЖ?
Качество жизни — весьма важный показатель для людей. Многие пациенты очень боятся таких серьезных операций как РПЭ, полагая, что, вылечив свое основное заболевание, будут потом жить неполноценной жизнью или, хуже того, станут инвалидами. Некоторые даже считают, что пусть я лучше поживу еще пару тройку лет, зато полноценной жизнью, чем после операции пусть и долго, зато буду сам мучиться и своих родственников обременять. К сожалению, такое расхожее мнение далеко от истины. Если не лечить онкологического больного, он довольно быстро начинает испытывать всю тяжесть своего заболевания, страдать от расстройств функции пораженных органов, мучиться от невыносимых болей, быстро превращаться в недееспособного инвалида, стремительно угасать на глазах родных и близких. В таком состоянии больной и сам страдает и заставляет страдать близких ему людей. Не лучше ли сделать все возможное для излечения?!
РПЭ дает больным ранними стадиями РПЖ великолепный шанс не только выжить, но и жить долгие годы практически полноценной жизнью. По данным немецких авторов J. Hodzic и соавт. (2003) 73% прооперированных удовлетворены или очень удовлетворены качеством жизни после радикальной простатэктомии, а 98% из них согласились бы перенести РПЭ вновь. Современная конформная (фокусированная) лучевая терапия и имплантация радиоактивных зерен в предстательную железу (брахитерапия) также обеспечивает пациентам достаточно хорошее качество жизни после их применения. Эти виды лучевой терапии примерно с такой же частотой, как и РПЭ, вызывают расстройства эрекции, и реже вызывают недержание мочи. Однако значительно чаще они вызывают такие неприятные симптомы, как учащенное и болезненное мочеиспускание (признаки лучевого цистита), а также расстройства стула и кровотечения из прямой кишки (признаки лучевого проктита). Данные осложнения современных видов лучевой терапии ранних стадий РПЖ делают качество жизни после них несколько хуже, чем после РПЭ (Stene JB, Angelsen A., 2003; Penson DF, Litwin MS., 2003). Безусловно, качество жизни больных после того или иного метода лечения зависит от квалификации и опыта врачей, их оснащения современным оборудованием, условиях в которых проводится наблюдение за пациентом после лечения. В условиях нашей страны, к сожалению, практически невозможно провести лучевую терапию ранних стадий РПЖ в соответствии с мировыми стандартами (в основном из-за отсутствия соответствующего оборудования и опыта врачей). Однако у нас есть специалисты, за плечами которых уже многие сотни выполненных операций РПЭ. А высочайшая квалификация и опыт хирурга имеет критически важное значение для того, насколько удачно пройдет послеоперационная реабилитация и насколько полноценной будет жизнь пациента после РПЭ (Downs T.M. и соавт., 2003).
В клинике Андрос накоплен достаточный опыт выполнения радикальных простатэктомий, излечивающих операций на ранних стадиях рака предстательной железы. Послеоперационная реабилитация в клинике осуществляется в соответствии с самыми передовыми стандартами медицины Западной Европы и США. Наши пациенты выписываются из стационара через 3 — 5 дней после операции, а через 3 — 4 недели после нее возвращаются к своей обычной жизни и работе. В случае развития любых осложнений после операции РПЭ специалисты клиники Андрос окажут самую квалифицированную помощь. В клинике доступны все современные методы лечения расстройств эрекции и недержания мочи. Выбирайте надежный путь к излечению от рака предстательной железы!
Список литературы
Если у Вас остались вопросы, Вы можете получить консультацию ведущих специалистов клиники Андрос.