С помощью чего на рабочем столе создаются асептические условия
Организация работы в асептических условиях
Источниками загрязнения стерильных растворов могут быть исходные вещества, окружающая среда, оборудование, тара, укупорочный материал, работающий персонал.
«Асептика— это определенные условия работы, комплекс организационных мероприятий, позволяющих в максимальной степени предохранить лекарства от попадания в них микроорганизмов».
Асептика включает в себя ряд последовательных мероприятий, пополняющих друг друга, и ошибка, допущенная в одном звене этого ряда, сводит на нет всю проведенную и последующую работу.
Асептические условия предусматривают наличие в аптеке особого помещения для приготовления стерильных и асептических лекарств — асептического блока, который должен иметь не менее трех комнат:
1. Предасептическая (шлюз) — предназначена для подготовки персонала к работе.
2. Асептическая — предназначена для приготовления лекарственных форм.
3. Аппаратная — в ней устанавливаются автоклавы, стерилизаторы, аппараты, позволяющие получать воду для инъекций.
Требования к помещению. Производство лекарств в асептических условиях осуществляется в «чистых» помещениях, в которых нормируется чистота воздуха по содержанию микробных и механических частиц.
Асептический блок обычно располагается вдали от источников загрязнения микроорганизмами (зала обслуживания больных, моечной, фасовочной, санитарного узла).
В помещениях для приготовления лекарств в асептических условиях стены должны быть окрашены масляной краской или выложены светлой кафельной плиткой, при этом не должно быть выступов, карнизов, трещин. Потолки окрашиваются клеевой или водоэмульсионной краской. Полы покрываются линолеумом или релином с обязательной сваркой швов. Двери и окна должны быть плотно подогнаны и не иметь щелей.
Асептический блок оборудуется приточно-вытяжной вентиляцией с преобладанием притока воздуха над вытяжкой. Для снижения микробной обсемененности рекомендуется установка воздухоочистителей, которые обеспечивают эффективную очистку воздуха фильтрацией через фильтры из ультратонких волокон и ультрафиолетовое облучение.
Для обеззараживания воздуха в асептическом блоке устанавливаются неэкранированные бактерицидные облучатели: настенные (ОБН-150), потолочные (ОБП-300), передвижные маячного типа (ОБПЕ-450); бактерицидные лампы БУВ-25, БУВ-30, БУВ-60 из расчета мощности 2—2,5 Вт на 1 м 3 объема помещения, которые включают на 1—2 часа до начала работы в отсутствие людей. Включатель для этих облучателей должен находиться перед входом в помещение и сблокирован со световым табло «Не входить, включен бактерицидный облучатель». Вход в помещение, где включена неэкранированная бактерицидная лампа, разрешается только после ее выключения, а длительное пребывание в указанном помещении — только через 15 минут после отключения неэкранированной бактерицидной лампы.
В присутствии персонала могут эксплуатироваться экранированные бактерицидные облучатели, которые устанавливаются на высоте 1,8—2 м, из расчета 1 Вт на 1 м 3 помещения при условии исключения направленного излучения на находящихся в помещении людей.
Поскольку ультрафиолетовые облучатели образуют в воздухе токсические продукты (озон и оксиды азота), при их работе вентиляция должна быть включена.
Все оборудование и мебель, вносимые в асептический блок, предварительно обрабатываются салфетками, смоченными дезинфицирующим раствором (раствор хлорамина Б 1 %-ный, раствор хлорамина Б 0,75 %-ный с 0,5% моющего средства, раствор водорода пероксида 3 %-ный с 0,5 % моющего средства). Хранение в асептическом блоке неиспользуемого оборудования категорически запрещается. Уборка асептического блока проводится не реже одного раза в смену с использованием дезинфицирующих средств.
Один раз в неделю проводится генеральная уборка асептического блока. При этом помещения по возможности освобождают от оборудования, моют и дезинфицируют стены, двери, полы. После дезинфекции облучают ультрафиолетовым светом.
Перед входом в помещение асептического блока должны быть резиновые коврики, которые один раз в смену смачиваются дезинфицирующим раствором. Асептический блок отделяется от других помещений аптеки воздушными шлюзами.
Санитарная одежда, халаты, марля, изделия из текстиля, вата стерилизуются в биксах в паровых стерилизаторах при температуре 132 °С в течение 20 минут или при 120 °С в течение 45 минут и хранятся в закрытых биксах не более 3 суток. Обувь перед началом и после окончания работы дезинфицируют снаружи и хранят в шлюзах. Лица с инфекционными заболеваниями, открытыми ранами на коже, носители патогенной микрофлоры до полного их выздоровления не должны допускаться к работе.
Требования к исходным веществам и материалам. Лекарственные вещества, необходимые для приготовления лекарств в асептических условиях, хранятся в шкафах в плотно закрывающихся штангласах в условиях, исключающих их загрязнение. Штангласы перед каждым заполнением моются и стерилизуются.
Для приготовления инъекционных лекарственных форм используют лекарственные вещества квалификации «химически чистый», «чистый для анализа» или «годен для инъекций», отвечающие требованиям нормативно-технической документации и ГФУ.
Однако к некоторым препаратам сорта «годен для инъекций» являются дополнительные требования по качеству (табл. 29).
Вспомогательные вещества (стабилизаторы, консерванты) по качеству также должны соответствовать требованиям нормативно-технической документации.
Вспомогательный материал (вата, марля, пергаментная бумага, фильтры и т. п.) стерилизуется в биксах или банках с притертыми пробками при температуре 132 °С в течение 20 минут или при 120 °С в течение 45 минут и хранится в закрытом виде не более 3 суток. Вскрытые материалы должны использоваться в течение 24 часов. После каждого забора материала бикс плотно закрывается. Забор производится стерильным пинцетом. При этом следует иметь в виду, что вспомогательный материал должен укладываться для стерилизации в биксы в готовом к применению виде.
Упаковка. Загрязнение растворов механическими частицами и микроорганизмами можно снизить путем качественной подготовки тары и укупорочных средств, а также соблюдением условий их хранения и транспортировки непосредственно на место разлива раствора. Аптечная посуда моется (посуда, бывшая в употреблении, предварительно дезинфицируется, затем моется) и стерилизуется, укупоривается и хранится в плотно закрывающихся шкафах, выкрашенных изнутри светлой масляной краской или покрытых пластиком (см. с. 100).
При мытье посуды, кроме удаления механических примесей, необходимо возможно полнее удалить растворимые щелочные соединения, которых особенно много в щелочном стекле. Мытье посуды с применением мыла мало пригодно, так как при этом может быть образование нерастворимого кальциевого мыла, загрязняющего стекло. Моющие и дезинфицирующие средства представлены в главе 8. Посуду моют вручную с помощью ерша или моечных машин, описание которых приведено в главе 10. Чистота вымытой посуды и полнота смываемости моющих средств должна контролироваться (см. главу 8, с. 104).
Инъекционные растворы, приготовляемые в аптеках, необходимо отпускать во флаконах из нейтрального стекла марки НС-1 (для мед препаратов, антибиотиков) и НС-2 (сосуды для крови). В порядке исключения после освобождения от щелочности используют флаконы из стекла марки АВ-1 и МТО, учитывая, что срок хранения растворов в них не должен превышать 2 суток, так как возможно выщелачивание стекла (см. главу 8, с. 96).
Для укупорки флаконов с инъекционными растворами используют пробки специальных сортов резины (с. 99—100): ИР-21 (силиконовая), 25П (натуральный каучук), 52-369, 52-369/1, 52-369/П (бутиловый каучук), ИР-119, ИР-119А (бутиловый каучук). В зарубежной литературе имеются сообщения о применении для укупорки инъекционных растворов пробок из поливинилхлорида.
Обработка, мытье и стерилизация пробок и алюминиевых колпачков представлены в главе 8, с. 103—104.
Требования к производственному оборудованию. Применение средств малой механизации при приготовлении растворов для инъекций допускается при условии возможности их обеззараживания или стерилизации (см. главу 10). Оборудование должно быть сконструировано и размещено так, чтобы обеспечивалась его подготовка к работе, эксплуатации и обслуживанию. Материал, из которого сделано хюрудование, не должен вступать в реакцию с компонентами лекарства, а конструкция оборудования должна исключать возможность попадания в лекарство веществ, используемых для его эксплуатации вещества, охлаждающие жидкости и т. п.).
Дата добавления: 2016-12-26 ; просмотров: 4044 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
СОЗДАНИЕ АСЕПТИЧЕСКИХ УСЛОВИЙ В АПТЕКЕ



Одним из важнейших требований при изготовлении стерильных растворов является соблюдение правил асептики.
Источниками микробиологического загрязнения лекарственных форм являются вентиляционный или атмосферный воздух, поверхности помещения, оборудования, вспомогательные материалы, технологическая спецодежда, обслуживающий персонал. В неочищенном воздухе во взвешенном состоянии может содержаться различное количество инородных включений размером: 0,03-0,3 мкм (бактерии и вирусы), 10-100 мкм (частицы пыли), 30-200 мкм (волокна, волосы). Известно также, что человек постоянно выделяет аэрозольные частицы, число которых колеблется от 1 тысячи до 30 миллионов в минуту, в зависимости от характера производимых им движений, состояния верхних дыхательных путей, интенсивности разговоров. Так, в положении стоя или сидя без всякого движения человек выделяет в окружающий воздух 1 миллион частиц в минуту размером ≥0,3 мкм; при движении – от 5 до 7,5 миллионов.
Для обеспечения асептических условий в соответствии с надлежащей аптечной практикой в аптеках первой категории организуют специальное помещение изготовления стерильных лекарственных средств (асептический блок со шлюзом). При осуществлении аптечного изготовления по индивидуальным назначениям (рецептам врача) и требованиям (заявкам) организации здравоохранения в количестве менее 50 рецептурных номеров в день стерильных лекарственных средств и лекарственных средств, изготавливаемых в асептических условиях, разрешается совмещение помещения аптечного изготовления лекарственных средств и асептического блока со шлюзом.
Изготовление других лекарственных форм в асептическом блоке не допускается. Перед входом в асептический блок должны быть резиновые коврики, смоченные дезинфицирующим раствором.
Передачу чистой посуды в асептическую комнату и флаконов с растворами под обкатку и стерилизацию осуществляют через передаточные окна, оснащенные бактерицидными лампами.
Шлюз предназначен для переодевания и обработки рук персонала. В шлюзе предусмотрены:
Ø шкаф для спецобуви, халата и биксов с комплектами стерильной одежды;
Ø раковина, оборудованная педальным краном или краном с локтевым приводом;
Ø принадлежности для обработки рук;
Ø воздушная электросушилка;
Стены помещений асептического блока должны быть окрашены масляной краской или выложены метлахской плиткой без трещин, выступов, карнизов. Потолки окрашивают клеевой или водоэмульсионной краской. Полы покрывают линолеумом или релином с обязательной сваркой швов. Столы покрывают пластиком. Двери и окна должны быть плотно подогнаны и не должны иметь щелей.
Асептический блок оборудуется приточно-вытяжной вентиляцией с преобладанием притока воздуха над вытяжкой. Воздух подают через простерилизованные бактериальные фильтры «Лайк» с тканью Петрянова. На фильтрах задерживаются пылевидные частицы, аэрозоли и микроорганизмы. Для снижения микробной обсемененности рекомендуется установка воздухоочистителей передвижных рециркуляционных ВОПР-0,9 и ВОПР-1,5.
Один раз в неделю производится генеральная уборка. При этом помещение по возможности освобождается от оборудования. Начинать уборку необходимо с асептической. Вначале моется потолок, затем стены и двери от потолка к полу. Движения должны быть плавными, обязательно сверху вниз.
Весь инвентарь для уборки асептического блока должен быть четко маркирован «Асептический блок» и должен храниться в специальном шкафу. Там же хранятся ветошь, щетки, которые после каждой уборки должны быть продезинфицированы, просушены и уложены в чистую промаркированную тару с плотной крышкой.
Персонал, работающий в асептическом блоке, должен соблюдать санитарные требования и правила работы в асептических условиях. Персоналу, не работающему в асептическом блоке, вход в это помещение категорически запрещен.
При входе в асептический блок персонал одевает специальную обувь. Обувь перед началом и после окончания работы дезинфицируют снаружи (2-х кратное протирание дезраствором).
Затем работники асептического блока моют руки теплой проточной водой с мылом (подарочное, банное, детское, хозяйственное) и щеткой в течение 1-2 мин. Предварительно щетки кипятят в течение 15 мин. в воде очищенной или в 20% растворе натрия гидрокарбоната.
Руки вытирают насухо, надевают халат, шапочку, четырехслойную марлевую повязку (которую меняют каждые 4 часа), бахилы. При этом одежда должна быть собрана на запястьях и высоко на шее. Не допускается наличие объемной одежды. Затем руки дезинфицируют дезраствором (0,5 % раствором хлорамина Б, 0,5% раствором хлоргексидина). Согласно 130 Приказа, руки протирают марлевой салфеткой, смоченной дезраствором. На обработанные руки персонала, занятого на участке разлива и укупорки раствора, должны быть надеты стерильные резиновые перчатки.
При работе в асептических условиях:
Ø запрещается вход в асептическую комнату в нестерильной одежде и выход из асептического блока в стерильной одежде; курить и принимать пищу; поднимать и повторно использовать предметы, упавшие на пол во время работы;
Ø следует ограничить разговоры и перемещения в асептическом блоке;
Ø рекомендуется носить короткую стрижку, при этом волосы должны быть убраны под плотно прилегающую шапочку или косынку; рекомендуется делать гигиенический маникюр без покрытия ногтей лаком, не пудриться до и во время работы, не носить ювелирные изделия, красить губы только жирной помадой;
Ø обо всех случаях заболевания ставить в известность администрацию.
Создание асептических условий в аптеке



Ваптеке изготовление лекарственных форм в условиях асептики осуществляется в соответствии с санитарными требованиями, изложенными в приказе МЗ РФ № 309 от 21.10.1997 г. и методических указаниях по изготовлению стерильных растворов в аптеках, утвержденных МЗ РФ 24.08.1994 г.
Для изготовления лекарственных форм в асептических условиях в аптеке оборудуется асептический блок, который включает помещения для изготовления, фасовки и стерилизации, а также получения воды для инъекций и отделен от других помещений аптеки шлюзом. Пол, стены и потолки всех помещений асептического блока должны быть отделаны материалом, позволяющим проводить влажную уборку с применением дезинфицирующих средств. Не допускается наличие выступов, карнизов во избежание скопления пыли.
Для предотвращения попадания воздуха извне окна и двери не должны иметь щелей, и в помещении должно поддерживаться небольшое избыточное давление приточного фильтрованного воздуха.
Быстрая и эффективная очистка воздуха достигается с помощью воздухоочистителей передвижных рециркуляционных (ВОПР). Очистка воздуха при их использовании достигается за счет фильтрации через фильтры из ультратонких волокон. С целью обеззараживания воздуха во всех помещениях асептического блока устанавливают бактерицидные облучатели. Они могут быть экранированные и неэкранированные. Последние включаются в отсутствии людей за 1-2 часа до начала работы. В присутствии персонала включаются только экранированные облучатели. В процессе работы всех ультрафиолетовых облучателей образуются азот и окислы азота, которые должны удаляться с помощью вентиляции.
Приказ № 309 рекомендует использовать в асептическом блоке аптек камеры или столы с ламинарным потоком воздуха.
Уборку помещений асептического блока проводят не реже 1 раза в смену в конце работы с использованием дезинфицирующих средств (хлорамина Б, гипохлорита натрия, пероксида водорода). 1 раз в неделю проводят генеральную уборку.
Создание асептических условий в аптеке предполагает также использование стерильного вспомогательного материала, средств укупорки и упаковки, стерилизацию вспомогательных и лекарственных средств, если они могут быть простерилизованы, использование для приготовления лекарственных форм воды для инъекций.
Особые требования предъявляются к персоналу асептического блока, который должен строго соблюдать правила личной гигиены, работать в специальной одежде, тщательно обрабатывать руки.
· работа в асептическом блоке;
· санитарная обработка помещений и оборудования;
· использование стерильного вспомогательного материала, средств укупорки и упаковки;
· применение воды для инъекций;
· использование специально обученного персонала.
Основным требованием к инъекционным растворам является стерильность. Стерильность обеспечивается асептическим приготовлением в асептическом блоке, а также последующей стерилизацией приготовленных растворов. Стерилизация – это процесс умерщвления в объекте или удаление из него микроорганизмов всех видов, находящихся на всех стадиях развития. Существует четыре фармакопейных метода стерилизации:
ü Термический (паровой и воздушный)
ü Химический (газовый и стерилизация растворами)
ü Стерилизация фильтрованием
ü Радиационный метод стерилизации
Изделия из стекла, фарфора, металла, полимерных материалов перед стерилизацией подвергают предстерилизационной очистке.
Термический метод стерилизации.
Паровой метод стерилизации осуществляют насыщенным водяным паром при избыточном давлении 0,11 МПа (1,1 кгс/см² и температуре 120 °С; 0,20 МПа (2 кгс/см² и температуре 132 °С.
Стерилизацию проводят в паровых стерилизаторах для достижения максимальной эффективности процесса стерилизации необходимо полное удаление воздуха из стерилизационной камеры и обрабатываемых объектов, а также правильное размещение последних, обеспечивающее свободное проникновение к ним пара.
Стерилизация паром при температуре 120 °С рекомендуется для растворов лекарственных веществ. Время стерилизационной выдержки зависит от физико-химических свойств препарата, объема раствора и используемого оборудования.
| Объём образца, мл. | Минимальное время стерилизационной выдержки, мин. |
| До 100 | |
| От 100 до 500 | |
| ≥ 500 ≥ 1000 |
Стерилизацию растворов лекарственных веществ для инъекций проводят в герметично укупоренных, предварительно простерилизованных флаконах или ампулах.
Жиры и масла в герметично укупоренных сосудах стерилизуют при 120 °С в течение 2 ч.
Этим методом стерилизуют также изделия из стекла, фарфора, металла, перевязочные и вспомогательные материалы. Время стерилизационной выдержки при температуре 120 °С 45 мин, при 132 °С 20 мин. для стерилизации изделий из резины следует использовать первый из указанных режимов.
Воздушный метод стерилизации осуществляют сухим горячим воздухом в воздушных стерилизаторах при температуре 160, 180 или 200 °С.
Эффективность этого метода стерилизации зависит от температуры, времени, степени теплопроводности стерилизуемых объектов и правильности расположения их внутри стерилизационной камеры для обеспечения свободной циркуляции горячего воздуха. Воздушный метод используют для стерилизации термостойких порошкообразных веществ (натрия хлорида, окиси цинка, талька, белой глины и др.).
| Масса образца, г | Температура, °С | Минимальное время стерилизационной выдержки, мин. |
| До 25 | ||
| От 25 до 100 | ||
| ≥ 100 ≥ 200 | ||
| Масса образца, г | Температура, °С | Минимальное время стерилизационной выдержки, мин. |
| До 100 | ||
| От 100 до 500 |
Изделия из стекла, металла, силиконовой резины, фарфора, установки для стерилизующего фильтрования с фильтрами и приемники фильтрата стерилизуют при 180 °С в течение 60 мин или при 160 °С в течение 2,5 ч.
Контроль параметров и эффективности термических методов стерилизации осуществляют с помощью контрольно-измерительных приборов, химических и биологических тестов.
В качестве химического теста стерилизации используют вещества, изменяющие свой цвет или физическое состояние при определенных параметрах стерилизации.
Бактериологический контроль осуществляют с помощью биотеста стерилизации.
Химический метод стерилизации.
Для газовой стерилизации используют окись этилена или ее смесь с различными флегматизаторами: бромистым метилом, двуокисью углерода, хладонами (фреонами) и др. Стерилизацию проводят в газовых стерилизаторах или микроанаэростатах (портативный аппарат) при следующих режимах:
— окись этилена — стерилизующая доза 1200 мг/дм³ температура стерилизации не менее 18°С, относительная влажность 80 %, время стерилизационной выдержки — 16 ч (портативный аппарат);
— смесь ОБ (смесь окиси этилена и бромистого метила в весовом соотношении 1:2,5):
а) стерилизующая доза 2000 мг/дм³ температура стерилизации 55 °С, относительная влажность 80 %, время стерилизационной выдержки — 4 ч;
б) стерилизующая доза 2000 мг/дм³ температура стерилизации не менее 18 °С время стерилизационной выдержки — 16 ч при той же относительной влажности (портативный аппарат).
Допускается использование других режимов газовой стерилизации, обеспечивающих стерильность и сохранность объекта. Режим должен быть обоснован и указан в нормативно-технической документации.
Стерилизуемые изделия упаковывают в пакеты из полиэтиленовой пленки толщиной от 0,06 до 0,2 мм, пергамента и др. Метод рекомендован для изделий из резины, полимерных материалов, стекла, металла.
В связи с токсичностью окиси этилена и бромистого метила применение стерилизованных этими газами изделий допускается только после их дегазации, т. е. выдержки в вентилируемом помещении до допустимых остаточных количеств, указанных в нормативно-технической документации.
Контроль параметров и эффективности газовой стерилизации осуществляют с помощью контрольно-измерительных приборов, химических и биологических тестов.
Для химической стерилизации растворами используют перекись водорода и надкислоты.
Эффективность стерилизации растворами зависит от концентрации активно действующего вещества, времени стерилизационной выдержки и температуры стерилизующего раствора.
При стерилизации 1 % раствором дезоксона-1 (по надуксусной кислоте) температура стерилизующего раствора должна быть не менее 18 °С, время стерилизационной выдержки — 4 мин.
Химическую стерилизацию растворами проводят в закрытых ёмкостях из стекла, пластмассы или емкостях, покрытых неповрежденной эмалью, при полном погружении изделия в раствор на время стерилизационной выдержки. После этого изделие должно быть промыто стерильной водой в асептических условиях.
Метод рекомендуется для изделий из полимерных материалов, резины, стекла, коррозионно-стойких металлов.
Контроль параметров стерилизации растворами химических препаратов проводят химическим и физическим методами, определяя содержание активного действующего вещества в исходном и рабочем растворах, а также температуру рабочего раствора.
Растворы термолабильных веществ стерилизуют фильтрованием с помощью мембранных и глубинных фильтров, задерживающих микроорганизмы и их споры. Мембранные фильтры характеризуются ситовым механизмом задержания и постоянным размером пор при эксплуатации. Максимальный диаметр пор стерилизующего мембранного фильтра не превышает 0,3 мкм.
Глубинные фильтры характеризуются сложным механизмом ржания (ситовым, адсорбционным, инерционным) и в большинстве случаев непостоянным размером пор.
При стерилизации фильтрованием перед стерилизующим фильтром и помещают один или несколько префильтров. Поры префильтра больше пор фильтра или равны им.
Продолжительность фильтрования не должна превышать 8 ч.
Стерилизацию фильтрованием и розлив раствора проводят в асептических условиях. Эффективность стерилизации фильтрованием проверяют прямым посевом пробы фильтрата в питательную среду.
Радиационный метод стерилизации.
Облучение объектов в конечной упаковке производят на гамма-установках, ускорителях электронов и других источниках ионизирующего излучения дозой 25 кГр (2,5 Мрад) или другими дозами в зависимости от конкретных условий (микробная обсемененность продукции до стерилизации, радиорезистентность контаминантов, величина коэффициента надежности стерилизации).
Радиационный метод стерилизации может быть рекомендован для изделий из пластмасс, изделий одноразового использования в упаковке, перевязочных материалов, некоторых лекарственных средств и других видов медицинской продукции
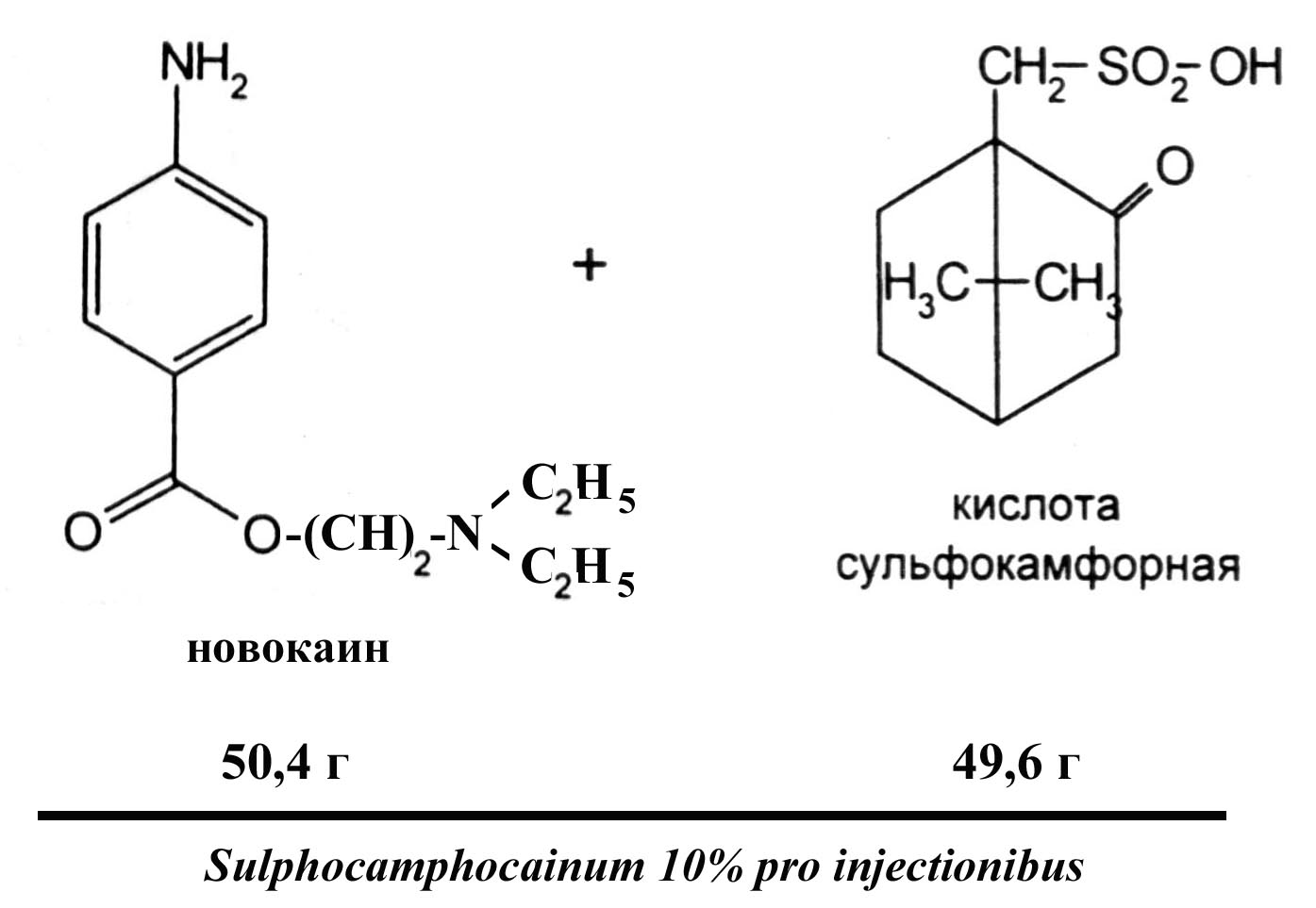
Смесь 49,6 г. сульфокамфорной кислоты и 50,4 г. новокаина (основания) доводят до 1 л водой для инъекции.