селективная дорсальная ризотомия при дцп что это
Нейрохирургическое отделение
Селективная дорзальная ризотомия в лечении детского церебрального паралича
Детский церебральный паралич считается одним из самых распространенных заболеваний у детей. ДЦП проявляется двигательными расстройствами, нарушением речи, равновесия, приступами судорог. Особенно значимым в клинической картине заболевания является тяжелое спастическое нарушение тонуса мышц.
Основной причиной детского церебрального паралича считается кислородное голодание. В результате чего в развивающемся мозге возникают необратимые изменения. Внутриутробные инфекции, преждевременное отделение плаценты, затяжные роды, несовместимость по группе крови или резусу могут стать фактором риска развития ДЦП. Недоношенные дети наиболее уязвимая группа для этой патологии.
Вызванное гипоксией или внутриродовой травмой повреждение мозга в итоге приводят к инвалидизации. Вот почему данная патология имеет социальное значение. Дети проходят длительную реабилитацию и с трудом учатся ходить, разговаривать, выполнять элементарные вещи.
В результате трудности передвижения большинство детей прикованы к инвалидным креслам.
Подходы к лечению ДЦП меняются с течением времени. Традиционное лечение ориентировано на ортопедический подход. Смысл его в том, чтобы используя хирургические и физиотерапевтические методы, добиваться удлиннения сухожилий пораженных мышц, и их расслабления. Постоянные курсы массажа, ботулотерапия, этапные гипсовые повязки, операции по удлинению сухожилий. Этот комплекс не дает стойкого результата и спустя некоторое время приходится все повторять. Ведь спастика не уходит, мышцы вновь сокращаются, что в итоге формирует контрактуры. Это замкнутый круг. Медикаментозное лечение также не дает стойкого эффекта.
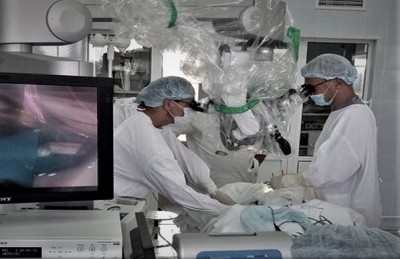
Есть подход, позволяющий стойко купировать спастику в нижних конечностях. Это Селективная дорзальная ризотомия. Применение микроскопической селективной сегментарной дорсальной ризотомии ведет к значительному уменьшению болевого синдрома и уменьшению непроизвольного напряжения мышц. Смысл операции в пересечении части спинномозговых корешков под контролем нейрофизиологического мониторинга. В результате разрывается порочный круг патологической импульсации, вызывающей патологически высокий тонус мышц. Эффект стойкий. Это снижает медикаментозную нагрузку, уменьшает болевой синдром, улучшает двигательные функции, облегчает уход за больным ребенком.
До недавних пор Липецкие дети имели ограниченную возможности получать подобную помощь. Дело в том, что подобные технологии только начинают осваиваться на просторах нашей страны. До последнего времени только федеральные центры, оснащенные по последнему слову техники, имели возможности проводить подобные высокотехнологические вмешательства. В последние годы очень существенное внимание уделяется медицинской помощи детям. Детская Областная больница оснастилась нейрохирургическим микроскопом, набором микрохирургического инструментария, аппаратом нейрофизиологического мониторинга. Это позволило освоить методику СДР и сделать доступной помощь детям с ДЦП. Первые операции в 2019 году проводились на нашей базе специалистами НИИ нейрохирургии им. Н.Н. Бурденко г. Москва. Затем своими силами. Всего выполнено 4 операции. В 2020 году планируется проведение не менее 5 операций селективной дорзальной ризотомии.
Подобные вмешательства требуют комплексного, мультидисциплинарного подхода. На всех этапах, начиная с обследования и заканчивая последующей реабилитацией, детьми занимаются квалифицированные неврологи, ортопеды и нейрохирурги. В перспективе на базе ГУЗ ОДБ планируется создание Центра лечения ДЦП регионального уровня.
врачи нейрохирурги: Васин Р.А., Красников М.А.
Селективная дорсальная ризотомия при дцп что это
Задняя селективная ризотомия — нейрохирургическая операция, выполняемая чаще всего на поясничном уровне для снижения патологического мышечного тонуса у больных с нижним спастическим парапарезом. Наиболее часто эта операция выполняется у больных со спастическими формами детского церебрального паралича (ДЦП) [1, 2]. Спастичностью называют зависящее от скорости растяжения усиление тонического стретч-рефлекса, возникающего в результате уменьшения тормозящего влияния на мотонейроны со стороны вышележащих структур [3]. Задняя селективная ризотомия снижает избыточную активность посредством чаcтичного рассечения задних корешков спинного мозга, в которых проходят миотатические волокона — пути, через которые замыкается стретч-рефлекс и реализуется спастический синдром [4]. В 2002 г. был проведен метаанализ ранних результатов ризотомии в 3 рандомизированных исследованиях. Было доказано, что в краткосрочном периоде (от 6 мес до 1 года) задняя селективная ризотомия приводит к снижению спастичности, увеличению объема движений, а также к улучшению локомоторных функций [5—7].
Отдаленные результаты ризотомии прослежены в литературе недостаточно четко, в основном показаны осложнения: деформации позвоночного столба и болевой синдром. По результатам исследования отдаленных результатов ризотомий начиная с 2011 г. были сделаны следующие выводы:
1) невозможно достоверно оценить функциональный результат, так как динамика локомоторного статуса в разных группах по шкале GMFM различна, поэтому динамику функций нужно оценивать отдельно для каждой группы;
2) функциональный результат следует оценивать отдельно в разных возрастных группах;
3) отдаленные осложнения ризотомии, например, такие как деформации позвоночного столба, могут быть не связаны с операцией, так как вообще характерны для больных ДЦП [8].
Проведенная в 1996 г. работа на базе института по исследованию результатов задней селективной ризотомии [1] подтвердила высокую эффективность вмешательства для коррекции патологического мышечного тонуса в отдаленном периоде. Однако работа была выполнена на небольшой серии больных, в работе не применялась оценка больных по глобальным двигательным шкалам. В отдаленном периоде отмечались осложнения в виде прогрессирования деформаций позвоночного столба, что могло объясняться использованием в качестве доступа ламинэктомии.
Цель настоящего исследования — систематизация и оценка отдаленных результатов задней селективной ризотомии у больных с ДЦП, относящихся к различным функциональным группам по шкале GMFM.
Материал и методы
Материал исследования составили 47 больных с ДЦП в форме нижнего спастического парапареза и тетрапареза (см. таблицу): 32 (68%) мальчика и 15 (32%) девочек, средний возраст — 7,4±6,1 года.

Все больные до операции проходили неоднократные курсы консервативного и реабилитационного лечения с незначительным и нестойким клиническим эффектом. Во всех случаях до операции больным проводили ботулинотерапию в спазмированные мышцы нижних конечностей (2—6 инъекций). У 16 больных клинический эффект отсутствовал, у 31 пациента отмечен парциальный клинический эффект, который по мере последующих инъекций регрессировал. В 5 случаях больным уже были выполнены ортопедические вмешательства по поводу фиксированных контрактур: ахиллопластика и удлинение сухожилий мышц hamstring-группы (задней группы мышц бедра).
Отбор больных для хирургического лечения проводился на основании комплексного обследования с участием невролога, физиотерапевта, ортопеда и нейрохирурга. Протокол обследования включал оценку мышечного тонуса по шкале Ashworth, оценку объема пассивных и активных движений, видеорегистрацию ходьбы и оценку локомоторного статуса по глобальной шкале GMFM-88. Шкала Ashworth предполагает градацию мышечного тонуса от 1 до 5 баллов, где за 1 балл принимается нормальное значение мышечного тонуса, а за 5 — максимальное, когда пассивные движения полностью невозможны. Шкала GMFM состоит из 88 стандартных двигательных тестов, каждый из которых в зависимости от степени выполнения градируется по 3-балльной шкале: 0 — отсутствие выполнения движений, 1 — попытка выполнения, 2 — частичное выполнение, 3 — полное выполнение. Сумма баллов отражается в процентном соотношении. Больные, набравшие 20% и менее, относятся к 5-й категории (наиболее тяжелая форма заболевания), от 20 до 40% — к 4-й, от 40 до 60% — к 3-й, от 60 до 80% — к 2-й, от 80 до 100% — к 1-й категории.
Всем больным до операции выполнялось МРТ головного мозга для оценки гидроцефалии и исключения сопутствующей интракраниальной патологии и МРТ поясничного отдела спинного мозга для определения уровня конуса. Контрольный осмотр проводился через 3, 6 и 12 мес после операции, а далее через каждый год.
Статистическую обработку данных выполняли с использованием программы SPSS Statictics 6.0. Применялся корреляционный анализ с использованием коэффициента корреляции (r) Пирсона для оценки силы связи между объемом пересекаемых фасцикул, с одной стороны, и динамикой спастичности и функции — с другой. Для анализа значимых различий между дооперационными и послеоперационными значениями мышечного тонуса и локомоторных функций в различных группах больных применяли непараметрический критерий (Т) Вилкоксона, учитывая малый размер выборки и отсутствие нормального распределения по критерию Колмогорова—Смирнова.
Все больные были включены в исследование с 2007 по 2014 г. Больные, оперированные позже, в исследование не включались, поскольку короткий срок катамнеза не позволял адекватно оценить динамику локомоторных функций. Критериями включения в исследования служили:
1) высокий мышечный тонус (3 балла и более по шкале Ashworth);
2) неэффективность консервативной терапии;
3) неэффективность ботулинотерапии.
К противопоказаниям для проведения ризотомии относились:
1) вторичная мышечная дистония;
2) гиперкинетический синдром;
3) соматические противопоказания.
Задержка психического развития не считалась противопоказанием для хирургического лечения.

При стандартном расположении конуса производилась костнопластическая ламинотомия на уровне Th12—L1. У 2 больных с фиксированным спинным мозгом ламинотомия производилась на уровне L3—L4. После вскрытия твердой мозговой оболочки визуализировался конус спинного мозга. Задний корешок L1 визуализировался в области корешкового отверстия и выделялся до уровня отхождения от заднелатеральной борозды спинного мозга. Далее, следуя по заднелатеральной борозде вниз, последовательно выделяли задние корешки L2—S1. Каждый корешок разделяли на несколько фасцикул. Далее фасцикулы подвергали интраоперационной электростимуляции моно- или биполярным стимулятором с частотой 5 Гц, длительностью импульса 0,1—0,2 мс, амплитудой 0,5—2 мА. При этом оценивали моторные ответы в ногах. Патологическими считались ответы, возникающие в разных мышечных группах либо с противоположной стороны. Фасцикулы, дающие подобные ответы, коагулировали на протяжении и пересекали (рис. 2).

Если при стимуляции фасцикул моторные ответы не регистрировались либо были низкоамплитудными, то такие фасцикулы оставляли интактными. В том случае, если при стимуляции корешка S1 возникали ответы в сфинктере, эти фасцикулы сохраняли интактными для профилактики развития нарушения функций тазовых органов. Корешок S2 во всех случаях сохраняли интактным. В общей сложности пересекали от 50 до 75% объема корешка. При установке костного блока на место производили расщепление дужек Th12—L1, осуществляли пропил в остистых отростках на глубину 2/3 их длины, после чего дужку надламывали. За счет этого устранялся диастаз между дужками и выпиленным костным блоком.
После операции профилактически больным на сутки оставляли мочевой катетер ввиду возможной задержки мочи. Для профилактики развития болевого синдрома в послеоперационном периоде на 4 дня больным назначали трамадол внутримышечно 3 раза в сутки. Вертикализация больных начиналась на 45-е сутки. В течение 3 мес больным рекомендовалось ношение поясничного корсета в положении сидя и лежа. По истечении этого срока выполняли контрольную спондилографию. При отсутствии прогрессирующих деформаций корсет снимали. Физиотерапевтические процедуры начинали выполнять после выписки больных из стационара. Спустя 3 мес после операции оценивали объем остаточных контрактур и решали вопрос о проведении ортопедохирургического лечения.
Результаты
В раннем послеоперационном периоде во всех случаях было отмечено снижение патологического мышечного тонуса в приводящих, икроножных мышцах, hamstring-группе в среднем от 4,34±0,53 перед операцией до 1,61±0,45 после операции (p 
Динамика мышечного тонуса по шкале Ashworth в этих подгруппах была сходной: 2,64 в 3-й категории (от 4,28±0,39 до 1,64±0,24); 2,84 в 4-й (от 4,61±0,5 до 1,77±0,69); 2,59 в 5-й категории (от 4,22±0,54 до 1,63±0,51) (рис. 4).

Наилучшие функциональные результаты были получены у детей в возрастной группе до 10 лет. Суммарная динамика локомоторного статуса составила от 29±14% перед операцией до 32±17% в отдаленном периоде (p
СДР — селективная дорсальная ризотомия и реабилитация
дорожная карта высокоээффективной реабилитации при хирургической помощи
Селективная дорсальная ризотомия (СДР) — это малоинвазивная операция на позвоночнике, которая может навсегда снизить спастичность нижних конечностей и стимулировать двигательное развитие у детей с церебральным параличом. Следует отметить, что эффективность СДР зависит от своевременной и целенаправленной реабилитации.
До вмешательства необходимо провести углубленное обследование специалистом-реабилитологом для полной оценки состояния и физических возможностей ребенка, включающее:
После операции многое изменится в организме ребенка, в том числе будет наблюдаться слабость спастичных мышц и мышц-антогонистов, сенсорные нарушения и в первую очередь — нарушение проприоцепции, т. е. ощущение относительного положения частей тела и их движения. Изменятся двигательные паттерны, двигательное взаимодействие верхней части туловища и нижних конечностей, распределение нагрузки в том числе и на суставы.
Комплексная реабилитация послеоперационного периода
Послеоперационная реабилитация должна быть подразделена на все нижеперечисленные направления, каждое из которых включает в себя определенные методики и упражнения, отвечающие поставленным целям. Вместе с этим, только междисциплинарный подход, принципы преемственности и постуральной коррекции, правильно составленный маршрут реабилитации помогут восстановить тонус организма и успешно закрепить послеоперационные результаты.
2. Растяжение мягких тканей
3. Увеличение силы и выносливости мышц
4. Формирование правильных образцов движения (поза, двигательные переходы, ходьба)
5. Дыхательная терапия (влияние на поддержание позы, двигательные переходы и ходьбу)
Физическая реабилитация будет начинаться с упражнений, направленных на растяжение мышц и облегчение движений. В раннем послеоперационном периоде упражнения будут пассивными, а по мере восстановления будет поощряться активное включение ребенка в процесс реабилитации. Функциональные тренировки будут направлены на увеличения силы, развитие баланса и выравнивание позы сидя и стоя, подготовку к самостоятельному стоянию, ходьбе, а также развитие двигательных переходов.
При поступлении на реабилитацию после СДР, а также после прохождения курса, специалистами центра проводится повторное обследование для оценки эффективность вмешательства и формирования программы для домашнего этапа реабилитации.
Для использования эффекта от СДР с целью формирования новых двигательных и функциональных возможностей ребенка рекомендуется проходить реабилитацию каждые 3-4 месяца.
Послеоперационные меры предосторожности в первые 6 недель:
Нейрохирург Дмитрий Зиненко: «Мы даем детям с ДЦП шанс на полноценную жизнь»
из открытых источников
Доктор рассказал о новых методиках лечения этого тяжелого заболевания
О детском церебральном параличе (ДЦП) слышал, наверное, каждый, но лишь немногие представляют себе всю гамму ощущений больных этим недугом. Чтобы понять, с чем сталкиваются такие детишки, напрягите изо всей силы хотя бы мышцы руки или ноги. Не расслабляйте минуту, две, три… Понравилось? А пациенты с ДЦП испытывают это ежесекундно. Круглосуточно. Годами.
До недавних пор реабилитация таких больных фактически заключалась в максимальном их приспособлении к приемлемому существованию в социуме, однако в настоящее время появились методики, позволяющие воздействовать на причину заболевания. Об этом мы беседуем с доктором медицинских наук, заведующим нейрохирургическим отделением «Научно-исследовательского клинического института педиатрии имени академика Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Дмитрием Зиненко.
— Дмитрий Юрьевич, давайте в начале нашего разговора вкратце расскажем читателям о том, что такое ДЦП.
— Детский церебральный паралич — заболевание, проявляющееся комплексом двигательных нарушений. Видимым проявлением болезни является осложненная координация движений и нарушение двигательной активности, вызванное «зажатостью» мышц. Если не вдаваться в тонкости, заболевание характеризуется «сборной солянкой» симптомов, у него могут быть разные клинические проявления. Встречаются пациенты как с повышенным мышечным тонусом, так и с пониженным. А может быть чередование повышенного и пониженного тонуса — так называемая дистония. Тяжесть состояния больного зависит от того, насколько распространен этот процесс — это быть может одна рука или нога, только ноги, или в процесс вовлечены мышцы всего организма.
— Каковы причины возникновения ДЦП?
— На возникновение заболевания оказывают влияние большое количество факторов. Чаще всего это связано с повреждением головного мозга в период беременности или в первый месяц жизни младенца, травмой во время родов. Как правило, речь идет о нарушениях кровообращения, приводящих к гипоксии и ишемии вещества головного мозга, то есть повреждаются пути коммуникации между корой головного мозга и всем остальным организмом.
В настоящий момент на тысячу родов приходится два ребенка с ДЦП, подавляющее большинство детей с таким диагнозом — дети, родившиеся раньше срока.
— Как часто при ДЦП страдают интеллектуальные функции?
— Конечно, в ряде случаев при данном заболевании поражается и кора головного мозга. Соответственно, могут быть нарушены когнитивные функции. Однако, вопреки бытующему убеждению об умственной неполноценности детей с ДЦП, процентов семьдесят из них имеют сохранный интеллект. В этом и сложность: дети осознают свой дефект, смотрят на здоровых сверстников и страдают не только физически, но и психологически, потому что с возрастом начинают ощущать ограниченность своих возможностей.
— Насколько пациентов с ДЦП вообще можно адаптировать к социуму, и когда этот процесс нужно начинать?
— Как и при любом заболевании: чем раньше начнется лечение, тем лучше для пациента и тем больше возможностей для успешной социальной адаптации. Почему? Если, например, у ребенка повышенный мышечный тонус (а таких детей порядка 80 процентов от общего числа больных), это приводит к тому, что капилляры сжимаются, вследствие чего нарушается питание мышцы. Из-за этого с годами мышечное волокно превращается в соединительную ткань и, соответственно, утрачивает свою функцию.
Вопрос о степени возможной адаптации сложен и многогранен. Исторически сложилось, что пациентами с ДЦП занимаются главным образом реабилитологи, имеющие в своем арсенале только консервативные методы лечения, направленные в основном на сглаживание последствий заболевания. А последние достижения функциональной нейрохирургии позволяют воздействовать на причину болезни, и это фактически открывает абсолютно новые горизонты в лечении детей с ДЦП и последующей социальной интеграции пациентов.
— О каких достижениях идет речь?
— Для начала немного теории. Любая мышца нашего организма, сокращаясь, отправляет в головной мозг импульс — сигнал о своем действии. Мозг анализирует эту информацию и дает сигнал к дальнейшим действиям. Этот импульс передают дорсальные (сенсорные) корешки. Однако при ДЦП информация не доходит до головного мозга, а сразу передается на двигательные корешки, так как мозг из-за повреждения теряет свою контрольную функцию и импульс, образно выражаясь, бегает по кругу, возвращаясь обратно в мышцу. Этим и объясняется спазм.
Ситуацию может исправить селективная дорсальная ризотомия — операция, в ходе которой для разобщения порочного круга частично пересекаются чувствительные корешки, в результате чего мышцы расслабляются. Представляете, ребенок просыпается после наркоза, а у него уже расслабленные ноги!
Сейчас мы стараемся оперировать детишек со спастикой в нижних конечностях в районе двух-трех лет. Могу сказать с уверенностью: даже хорошо проведенная в более старшем возрасте (например, в восемь лет) операция не даст того эффекта, который мы могли бы получить при раннем вмешательстве. Это связано не только с перерождением мышц в соединительную ткань, но и с тем, что за годы у ребенка формируется патологический стереотип движения. То есть, после операции во многих случаях он получает возможность нормально ходить, но научить его этому уже не в пример тяжелее.
— Для каких пациентов с ДЦП этот метод лечения может быть наиболее эффективен?
— Существует пять функциональных классов ДЦП; у детей с первыми тремя, как правило, мы имеем сохранный интеллект, то есть их можно обучать. После операции они под руководством реабилитолога учатся использовать свои мышцы, самостоятельно двигаться. Иными словами, хирург в данном случае создает совершенно новые условия для жизни ребенка.
Дети с четвертым-пятым уровнями практически не коммуницируют, и в подавляющем большинстве случаев обучить их чему-либо невозможно. Но это не значит, что они не страдают от болей, от контрактур, от пролежней. Они лежат зажатые, с деформированными конечностями из-за спастики, в вынужденных позах. Мы делаем операции и таким детишкам, тем самым избавляя их от страданий и облегчая уход за ними.
Наиболее эффективна селективная дорсальная ризотомия при спастике ног. С руками несколько сложнее: в этом случае приходится идти в шейный отдел позвоночника, где у нас возможности ограничены. А ведь есть еще дети, у которых спазмированы и мышцы конечностей, и туловища, и оральная мускулатура — они даже говорить не могут.
В этом случае мы устанавливаем на переднюю брюшную стенку баклофеновую помпу — специальное устройство, являющееся, по сути, резервуаром для препарата, подающегося через специальный катетер в спинномозговой канал и блокирующего те самые патологические импульсы дорсальных корешков, приводящие к спазму мышц. Существует возможность индивидуальной регулировки дозы препарата, для каждого пациента она подбирается сообразно его состоянию. В среднем раз в полгода баклофеновую помпу необходимо заправлять — это безболезненная процедура, которая проводится в условиях стационара.
С помощью данной технологии спастический синдром можно устранить практически полностью, что открывает ребенку путь к полноценной жизни. Можно под руководством реабилитолога развивать мелкую моторику, что, в свою очередь, способствует развитию речи. И, как в случае с селективной дорсальной ризотомией: чем раньше начато лечение, тем лучше результат. Данную методику мы имеем возможность применять с любого возраста, иногда даже до года.
Третий метод, который мы применяем — установка в головной мозг специальных электродов, которые соединены с «зарядным устройством», вживляемым под кожу. Устройство имеет чип, с помощью которого можно регулировать работу электродов. Место установки, то есть конкретный очаг поражения, вычисляется с помощью МРТ.
Селективная дорсальная ризотомия показана при спастике, баклофеновую помпу и электроды можно применять, в том числе, и при дистонии. А вот лечить пониженный мышечный тонус нейрохирурги пока не научились. Впрочем, нужно отметить, что примерно 70–80 процентов случаев ДЦП связаны именно с повышенным тонусом мышц.
— Дмитрий Юрьевич, получается, в настоящий момент российская медицина обладает технологиями, которые позволяют если не вылечить, то существенно облегчить жизнь 70–80 процентам пациентов с ДЦП. Однако в реальности все происходит иначе. Почему?
— Одна из причин, думаю, в настороженном отношении к новым методикам. Хотя новыми их можно назвать весьма условно: за рубежом они применяются более 20 лет. Впрочем, какой смысл гадать о причинах? Изложу факты: на год нам дается порядка тысячи квот, а детей с ДЦП в России — более ста тысяч. А ведь нейрохирурги в данном случае могли бы не только помочь огромному количеству людей, но и сэкономить значительные средства для государственного бюджета. Расчеты простые: например, стоимость селективной дорзальной ризотомии — порядка 300 тысяч рублей, она может быть показана 20–30 процентам детей с ДЦП. Затем полтора-два года реабилитации, и пациент имеет шанс на полноценную жизнь: он может обучаться, социализироваться, приносить впоследствии пользу обществу. Похожим образом дела обстоят и с применением других нейрохирургических методик. При этом содержание одного ребенка с ДЦП обходится государству в среднем около 3 млн рублей в год; а ведь консервативное лечение в данном случае дает лишь временный эффект, и его необходимо повторять раз за разом. Добавьте сюда же средства на оплату больничных родителям таких детишек…
Ситуация получается какая-то странная: государство тратит безумные деньги на реабилитацию детей с ДЦП, вместо того чтобы выделить средства на хирургическое лечение. Понятно, что мы не вылечим всех больных ребятишек, но помочь 60–70 процентов из них вполне возможно.