серная кислота что делает
Серная кислота
Серная кислота
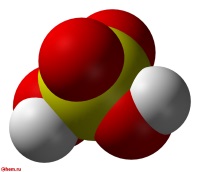
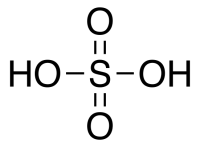
Строение молекулы и физические свойства
Серная кислота H2SO4 – это сильная кислота, двухосновная, прочная и нелетучая. При обычных условиях серная кислота – тяжелая маслянистая жидкость, хорошо растворимая в воде.
Растворение серной кислоты в воде сопровождается выделением значительного количества кислоты. Поэтому по правилам безопасности в лаборатории при смешивании серной кислоты и воды мы добавляем серную кислоту в воду небольшими порциями при постоянном перемешивании.
Валентность серы в серной кислоте равна VI.
Способы получения
1. Серную кислоту в промышленности производят из серы, сульфидов металлов, сероводорода и др. Один из вариантов — производство серной кислоты из пирита FeS2.
Основные стадии получения серной кислоты :
Рассмотрим основные аппараты, используемые при производстве серной кислоты из пирита (контактный метод):
| Аппарат | Назначение и уравнения реакций |
| Печь для обжига | 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q Измельченный очищенный пирит сверху засыпают в печь для обжига в «кипящем слое». Снизу (принцип противотока) пропускают воздух, обогащенный кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 800 о С |
| Циклон | Из печи выходит печной газ, который состоит из SO2, кислорода, паров воды и мельчайших частиц оксида железа. Такой печной газ очищают от примесей. Очистку печного газа проводят в два этапа. Первый этап — очистка газа в циклоне. При этом за счет центробежной силы твердые частички ссыпаются вниз. |
| Электрофильтр | Второй этап очистки газа проводится в электрофильтрах. При этом используется электростатическое притяжение, частицы огарка прилипают к наэлектризованным пластинам электрофильтра). |
| Сушильная башня | Осушку печного газа проводят в сушильной башне – снизу вверх поднимается печной газ, а сверху вниз льется концентрированная серная кислота. |
| Теплообменник | Очищенный обжиговый газ перед поступлением в контактный аппарат нагревают за счет теплоты газов, выходящих из контактного аппарата. |
| Контактный аппарат | 2SO2 + O2 ↔ 2SO3 + Q В контактном аппарате производится окисление сернистого газа до серного ангидрида. Процесс является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой реакции (получения SO3): Как только смесь оксида серы и кислорода достигнет слоев катализатора, начинается процесс окисления SO2 в SO3. Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню. |
| Поглотительная башня | Получение H2SO4 протекает в поглотительной башне. Однако, если для поглощения оксида серы использовать воду, то образуется серная кислота в виде тумана, состоящего из мельчайших капелек серной кислоты. Для того, чтобы не образовывался сернокислотный туман, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3. Образовавшийся олеум сливают в металлические резервуары и отправляют на склад. Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю. |
Общие научные принципы химического производства:
Химические свойства
1. Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени:
По второй ступени серная кислота диссоциирует частично, ведет себя, как кислота средней силы:
HSO4 – ⇄ H + + SO4 2–
2. Серная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Еще пример : при взаимодействии серной кислоты с гидроксидом калия образуются сульфаты или гидросульфаты:
Серная кислота взаимодействует с амфотерным гидроксидом алюминия:
3. Серная кислота вытесняет более слабые из солей в растворе (карбонаты, сульфиды и др.). Также серная кислота вытесняет летучие кислоты из их солей (кроме солей HBr и HI).
Или с силикатом натрия:
Концентрированная серная кислота реагирует с твердым нитратом натрия. При этом менее летучая серная кислота вытесняет азотную кислоту:
4. Т акже серная кислота вступает в обменные реакции с солями.
5. Разбавленная серная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Серная кислота взаимодействует с аммиаком с образованием солей аммония:
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании реакция возможна.
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
При взаимодействии с щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
6. Качественная реакция на сульфат-ионы – взаимодействие с растворимыми солями бария. При этом образуется белый кристаллический осадок сульфата бария:
Видеоопыт взаимодействия хлорида бария и сульфата натрия в растворе (качественная реакция на сульфат-ион) можно посмотреть здесь.
7. Окислительные свойства концентрированной серной кислоты проявляются и при взаимодействии с неметаллами.
Уже при комнатной температуре концентрированная серная кислота окисляет галогеноводороды и сероводород:
Назначение и применение серной кислоты
Многие считают, что серная кислота является очень опасной для человека. При непосредственном взаимодействии так оно и есть. Этот продукт активно используется в разных отраслях, так как обладает отличными эксплуатационными характеристиками. Компания «Химия и Технология» предоставляет приобрести серную кислоту на выгодных условиях.
Продукт отличается маслянистой структурой и прозрачностью, обладает достаточно резким запахом. В чистом виде является бесцветным, а дополнительный оттенок указывает на появление определённых соединений. Легко соединяется с водой, выделяя при этом теплоту в больших количествах.
Серная кислота считается мощным окислителем. Активно используется в разных промышленных отраслях. Применяется при изготовлении удобрений, солей и кислот, всевозможных красителей, в металлургической и нефтяной отрасли. Пищевая индустрия также используется серную кислоту.
Высококонцентрированное соединение вещества активно реагирует с водой. Поэтому нужно разбавлять химическую жидкость водой, а не наоборот.
Она хорошо поглощает пары жидкости из воздуха, поэтому используется для осушения газов. По причине низкой летучести, используется для вытеснения летучих кислот из солей. После чего образуются гидраты серной кислоты.
Как упоминалось выше, в высокой концентрации кислота является серьёзным окислителем. Она воздействует на разные металлы, а продукты реакции зависят от активности металла, образуя два ряда солей. В разбавленном виде вещество также взаимодействует с металлами, только без характерных окислительных свойств.
В промышленной индустрии этот химический элемент получают несколькими способами: контактным и нитрозным. Существует несколько видов – аккумуляторная (чистая), техническая и другие.
Применяется при изготовлении удобрений и в качестве аккумуляторного электролита. Используется в красителях и моющих средствах, пластиках и прочих реактивах, при обогащении руд и для очищения нефтепродуктов. В текстильной и фармацевтической отрасли также не обходятся без серной кислоты.
Серная кислота (Е513)

Изучение серной кислоты
Первые письменные упоминания о необычном веществе были в трудах арабских алхимиков Хайяна и Джабира. Они отметили, что некоторые кислые газы можно невозбранно получать, если прокаливать железный купорос или квасцы. Впоследствии около IX века опыт с прокаливанием проводил алхимик Ар-Рази. Он прокаливал смесь медного и железного купоросов, получив на выходе слабый раствор серной кислоты. После крестовых походов знания Ар-Рази попали в Европу. Уже в XIII веке алхимик Альберт Магнус сумел усовершенствовать этот способ получения кислоты, которая спустя несколько веков стала пищевой добавкой E513.
Параллельно с Магнусом свои труды проводил и алхимик Валентин. Он заметил, что при сжигании смешанных в порошкообразном виде селитры и серы образуется газ, серный ангидрид. Если его поглощает вода, то образуется серная кислота. Этот способ производства был популярен в Советском Союзом до 1955 года. Тогда для изготовления использовались камеры, облицованные свинцом (этот металл в серной кислоте не растворяется).
Спустя два столетия после Валентина и Альберта Магнуса алхимикам удалось добыть серную кислоты из серного колчедана. Этот материал был более распространённым, чем сера, что на 300 лет вперёд закрепило способ производства серы из пирита как основной. В наше время вещество также может производиться окислением оксида серы и его растворением в 70-процентном растворе уже готовой кислоты. Побочным продуктом реакции является олеум.
Свойства эмульгатора E513
В современной пищевой промышленности добавка E513 используется в качестве стабилизатора. Кроме соединения серы и селитры, в лабораторных условиях производство серной кислоты проводится следующим образом: сначала проводится обжиг железного колчедана, в результате которого на выходе получается соединение серы и водорода. Окисление этого соединения становится причиной образования серного ангидрида, который, растворяясь в воде, дает серную кислоту.
Вещество имеет высокие гигроскопические характеристики. При попадании на бумагу и древесину она вызывает обугливание, а при попадании на человеческую кожу становится причиной ожогов. Такие ее качества являются причиной повышенных требований безопасности при упаковке и перевозке. Пищевую добавку E513 допускается перевозить в таких емкостях:
Основные производители добавки E513

Применение серной кислоты
Конечно, в концентрированном виде серная кислота в пищевой промышленности не используется. Применяется только её 10-процентный раствор. Главным образом, добавку E513 используют в качестве подкислителя дрожжевого сусла. Этот подкислитель необходим в процессе приготовления спирта из крахмалосодержащего сырья. Нельзя забывать и о том, что данное вещество является хорошим регулятором кислотности в безалкогольных напитках, а также катализатором инверсии сахаров (в данном случае применяется E513 крайне редко).
Эмульгатор E513 прекрасно подходит для обработки загрязнённых дрожжей. Кислота буквально выжигает посторонние микроорганизмы, не разрушая при этом дрожжевую структуру. Используется она при рафинации жиров.
Пищевая промышленность – это не единственная сфера, где она нашла своё широкое применение. В сельском хозяйстве без неё тоже трудно обойтись. Её активно используют в изготовлении минеральных удобрений: так, вещество является важным элементом в образовании минеральных кислот и солей. Используется она и в тяжёлой промышленности, где она является электролитом в свинцовых батареях.
Польза и вред серной кислоты для человека
Наверное, каждый понимает, что любая кислота отрицательно влияет на человеческий организм и вообще любое живое существо. Ясно, что контакт концентрированного вещества, допустим, с кожей приводит к моментальному отмиранию и обугливанию кожи. Пары этого вещества повреждают дыхательные органы, что приводит к мучительной смерти. Повреждение слизистых оболочек, химические ожоги и прочие негативные воздействия реальны даже в случае контакта с популярным десятипроцентным раствором серной кислоты.
Работа с серной кислотой на производстве должна проводиться исключительно в специальных защитных костюмах, а также при наличии дополнительной защиты от воздействия эмульгатора. Если не придерживаться правил безопасности, то эмульгатор может вызвать такие заболевания дыхательной системы, как ларингит, бронхит, трахеит и прочее.
Эмульгатор E513 не относится к тем пищевым добавкам, которые можно найти в составе некоторых пищевых продуктов. В любом случае вреда от этой добавки значительно меньше, чем от тех добавок, которые запрещены в странах Запада и в России.
Законодательное регулирование использования добавки E513
В большинстве стран Евросоюза и СНГ (в том числе, в Украине и России) серную кислоту использовать в качестве пищевой добавки разрешено.
Серная кислота и последствия отравления ее парами. Справка
Серная кислота – сильная двухосновная кислота, в стандартных условиях представляет собой маслянистую жидкость без цвета и запаха. Неочищенная серная кислота имеет желтоватый или буро-желтый цвет. В технике серной кислотой называют ее смеси как с водой, так и с серным ангидридом.
Основные физические свойства: температура плавления – 10,38 °C; температура кипения – 279,6 °C; плотность вещества – 1,8356 граммов на кубический сантиметр.
Смешивается с водой во всех соотношениях г/100 мл. Концентрированная серная кислота является сильным окислителем. Разбавленная серная кислота взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода (H), с выделением Н2, окислительные свойства для нее нехарактерны.
Серную кислоту применяют: в производстве минеральных удобрений; как электролит в свинцовых аккумуляторах; для получения различных минеральных кислот и солей; в производстве химических волокон, красителей, дымообразующих и взрывчатых веществ; в нефтяной, металлообрабатывающей, текстильной, кожевенной отраслях промышленности; в пищевой промышленности (зарегистрирована в качестве пищевой добавки E513 (эмульгатор); в промышленном органическом синтезе.
Самый крупный потребитель серной кислоты – производство минеральных удобрений (в частности, фосфорных). Поэтому сернокислотные заводы стремятся строить в комплексе с заводами по производству минеральных удобрений.
При отравлении парами серной кислоты возникает раздражение и ожог глаз, слизистых оболочек носоглотки, гортани, носовые кровотечения, боль в горле, охриплость голоса из-за спазма голосовой щели. При этом особенно опасны отеки гортани и легких.
При попадании серной кислоты на кожу возникают химические ожоги, глубина и тяжесть которых определяются концентрацией кислоты и площадью ожога.
При поступлении серной кислоты внутрь немедленно после приема появляются резкие боли в области рта и всего пищеварительного тракта, сильная рвота с примесью сначала алой крови, а затем бурыми массами. Одновременно с рвотой начинается сильный кашель. Развивается резкий отек гортани и голосовых связок, вызывающий резкие затруднения дыхания. Кожа лица принимает темно-синий цвет, зрачки расширяются. Отмечается падение и ослабление сердечной деятельности.
Смертельная доза серной кислоты при поступлении внутрь – 5 миллиграммов.
При отравлении парами серной кислоты первая помощь состоит в обеспечении пострадавшему свежего воздуха. Необходимо промыть рот и зев раствором соды (20 грамм питьевой соды на 1 литр воды).
При попадании паров или капель серной кислоты на кожу пораженное место обильно промывают водой.
При поступлении серной кислоты внутрь необходимо осторожное промывание желудка, затем больной должен принимать жженую магнезию или известковую воду через 5 минут по 1 столовой ложке. Полезно обильное питье воды со льдом или молока, сырой яичный белок, жиры и масла, слизистые отвары.
Материал подготовлен на основе информации открытых источников
Серная кислота ГОСТ 4204-77
наименование
Серная кислота H 2 SO 4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O 1 — раствор SO3 в серной кислоте (олеум).
Содержание
Название
В XVIII—XIX веках серу для пороха производили из серного колчедана (пирит) на купоросных заводах. Серную кислоту в то время называли «купоросным маслом», очевидно отсюда происхождение названия её солей (а точнее именно кристаллогидратов) — купоросы.
Получение серной кислоты
Промышленный (контактный) способ
В промышленности серную кислоту получают окислением диоксида серы (сернистый газ, образующийся в процессе сжигания серы или серного колчедана) до триоксида (серного ангидрида) с последующим взаимодействием SO3 с водой. Получаемую данным способом серную кислоту также называют контактной (концентрация 92-94 %).
Нитрозный (башенный) способ
Раньше серную кислоту получали исключительно нитрозным методом в специальных башнях, а кислоту называли башенной (концентрация 75 %). Сущность этого метода заключается в окислении диоксида серы диоксидом азота в присутствии воды. Именно таким способом произошла реакция в воздухе Лондона во время Великого смога.
Другой способ
Сульфиды данных металлов обладают высочайшей прочностью, а также отличительным чёрным окрасом,
но могут быть окислены до сульфатов, например, азотной кислотой при кипении:
CuS + 8HNO3 → CuSO4 + 8NO2↑ + 4H2O
Физические и физико-химические свойства
Олеум
Растворы серного ангидрида SO3 в серной кислоте называются олеумом, они образуют два соединения H2SO4·SO3 и H2SO4·2SO3.
Олеум содержит также пиросерные кислоты, получающиеся по реакциям:
Температура кипения водных растворов серной кислоты повышается с ростом её концентрации и достигает максимума при содержании 98,3 % H2SO4.
| Содержание % по массе | Плотность при 20 ℃, г/см³ | Температура плавления, ℃ | Температура кипения, ℃ | |
|---|---|---|---|---|
| H2SO4 | SO3 (свободный) | |||
| 10 | — | 1,0661 | −5,5 | 102,0 |
| 20 | — | 1,1394 | −19,0 | 104,4 |
| 40 | — | 1,3028 | −65,2 | 113,9 |
| 60 | — | 1,4983 | −25,8 | 141,8 |
| 80 | — | 1,7272 | −3,0 | 210,2 |
| 98 | — | 1,8365 | 0,1 | 332,4 |
| 100 | — | 1,8305 | 10,4 | 296,2 |
| 104,5 | 20 | 1,8968 | −11,0 | 166,6 |
| 109 | 40 | 1,9611 | 33,3 | 100,6 |
| 113,5 | 60 | 2,0012 | 7,1 | 69,8 |
| 118,0 | 80 | 1,9947 | 16,9 | 55,0 |
| 122,5 | 100 | 1,9203 | 16,8 | 44,7 |
Температура кипения олеума с увеличением содержания SO3 понижается. При увеличении концентрации водных растворов серной кислоты общее давление пара над растворами понижается и при содержании 98,3 % H2SO4 достигает минимума. С увеличением концентрации SO3 в олеуме общее давление пара над ним повышается. Давление пара над водными растворами серной кислоты и олеума можно вычислить по уравнению:
величины коэффициентов А и В зависят от концентрации серной кислоты. Пар над водными растворами серной кислоты состоит из смеси паров воды, H2SO4 и SO3, при этом состав пара отличается от состава жидкости при всех концентрациях серной кислоты, кроме соответствующей азеотропной смеси.
С повышением температуры усиливается диссоциация:
При нормальном давлении степень диссоциации: 10⁻⁵ (373 К), 2,5 (473 К), 27,1 (573 К), 69,1 (673 К).
Плотность 100%-ной серной кислоты можно определить по уравнению:
d = 1,851 7 − 1,1 ⋅ 10 −3 t + 2 ⋅ 10 −6 t 2
С повышением концентрации растворов серной кислоты их теплоемкость уменьшается и достигает минимума для 100%-ной серной кислоты, теплоемкость олеума с повышением содержания SO3 увеличивается.
При повышении концентрации и понижении температуры теплопроводность λ уменьшается:
λ = 0,518 + 0,0016t − ( 0,25 + t/1293 ) ⋅ C/100
где С — концентрация серной кислоты, в %.
Максимальную вязкость имеет олеум H2SO4·SO3, с повышением температуры η снижается. Электрическое сопротивление серной кислоты минимально при концентрации SO3 и 92 % H2SO4 и максимально при концентрации 84 и 99,8 % H2SO4. Для олеума минимальное ρ при концентрации 10 % SO3. С повышением температуры ρ серной кислоты увеличивается. Диэлектрическая проницаемость 100%-ной серной кислоты 101 (298,15 К), 122 (281,15 К); криоскопическая постоянная 6,12, эбулиоскопическая постоянная 5,33; коэффициент диффузии пара серной кислоты в воздухе изменяется в зависимости от температуры; D = 1,67·10⁻⁵T 3/2 см²/с.
Химические свойства
Серная кислота в концентрированном виде при нагревании — довольно сильный окислитель.
Окисляет HI и частично HBr до свободных галогенов.
Углерод до CO2, серу — до SO2.
Окисляет многие металлы (исключения: Au, Pt, Ir, Rh, Ta.). При этом концентрированная серная кислота восстанавливается до SO2, например:
На холоде в концентрированной серной кислоте Fe, Al, Cr, Co, Ni, Ba пассивируются и реакции не протекают.
Наиболее сильными восстановителями концентрированная серная кислота восстанавливается до S и H2S. Концентрированная серная кислота поглощает водяные пары, поэтому она применяется для сушки газов, жидкостей и твёрдых тел, например, в эксикаторах. Однако концентрированная H2SO4 частично восстанавливается водородом, из-за чего не может применяться для его сушки. Отщепляя воду от органических соединений и оставляя при этом чёрный углерод (уголь), концентрированная серная кислота приводит к обугливанию древесины, сахара и других веществ.
Разбавленная H2SO4 взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода с его выделением, например:
Окислительные свойства для разбавленной H2SO4 нехарактерны. Серная кислота образует два ряда солей: средние — сульфаты и кислые — гидросульфаты, а также эфиры. Известны пероксомоносерная (или кислота Каро) H2SO5 и пероксодисерная H2S2O8 кислоты.
Серная кислота реагирует также с основными оксидами, образуя сульфат и воду:
На металлообрабатывающих заводах раствор серной кислоты применяют для удаления слоя оксида металла с поверхности металлических изделий, подвергающихся в процессе изготовления сильному нагреванию. Так, оксид железа удаляется с поверхности листового железа действием нагретого раствора серной кислоты:
Концентрированная H2SO4 превращает некоторые органические вещества в другие соединения углерода:
Качественной реакцией на серную кислоту и её растворимые соли является их взаимодействие с растворимыми солями бария, при котором образуется белый осадок сульфата бария, нерастворимый в воде и кислотах, например:
Применение
Серную кислоту применяют:
Мировое производство серной кислоты около 200 млн тонн в год. Самый крупный потребитель серной кислоты — производство минеральных удобрений. На P₂O₅ фосфорных удобрений расходуется в 2,2—3,4 раза больше по массе серной кислоты, а на (NH₄)₂SO₄ серной кислоты 75 % от массы расходуемого (NH₄)₂SO₄. Поэтому сернокислотные заводы стремятся строить в комплексе с заводами по производству минеральных удобрений.
Токсическое действие
Исторические сведения
Серная кислота известна с древности, встречаясь в природе в свободном виде, например, в виде озёр вблизи вулканов. Возможно, первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса «зеленого камня», встречается в сочинениях, приписываемых арабскому алхимику Джабир ибн Хайяну.
В IX веке персидский алхимик Ар-Рази, прокаливая смесь железного и медного купороса (FeSO4•7H2O и CuSO4•5H2O), также получил раствор серной кислоты. Этот способ усовершенствовал европейский алхимик Альберт Магнус, живший в XIII веке.
Схема получения серной кислоты из железного купороса — термическое разложение сульфата железа (II) с последующим охлаждением смеси
В трудах алхимика Валентина (XIII в) описывается способ получения серной кислоты путём поглощения водой газа (серный ангидрид), выделяющегося при сжигании смеси порошков серы и селитры. Впоследствии этот способ лег в основу т. н. «камерного» способа, осуществляемого в небольших камерах, облицованных свинцом, который не растворяется в серной кислоте. В СССР такой способ просуществовал вплоть до 1955 г.
Алхимикам XV в известен был также способ получения серной кислоты из пирита — серного колчедана, более дешевого и распространенного сырья, чем сера. Таким способом получали серную кислоту на протяжении 300 лет, небольшими количествами в стеклянных ретортах. Впоследствии, в связи с развитием катализа этот метод вытеснил камерный способ синтеза серной кислоты. В настоящее время серную кислоту получают каталитическим окислением (на V2O5) оксида серы (IV) в оксид серы (VI), и последующим растворением оксида серы (VI) в 70 % серной кислоте с образованием олеума.
В России производство серной кислоты впервые было организовано в 1805 году под Москвой в Звенигородском уезде. В 1913 году Россия по производству серной кислоты занимала 13 место в мире.