Реинфекция что это такое у детей
Иммунодефицит у ребенка
Содержание статьи
Такой диагноз у детей означает, что поражен один или несколько элементов системы иммунитета. При такой патологии тяжело протекают инфекционные заболевания, часто проявляются аутоиммунные болезни, возникают опухоли, могут быть аллергии.
Виды заболеваний
Данный синдром может быть как первичным (генетически обусловленным), так и вторичным (появляется ввиду внешних факторов или заболеваний).
Первичный иммунодефицит у детей – что это и откуда берется?
Врожденный иммунодефицит (ИД) у ребенка – это то, что развивается из-за генетических факторов, это первичные нарушения работы иммунной системы. В результате развиваются тяжелые инфекции, быстро переходящие в хроническую форму, а органы и ткани поражаются воспалительными процессами. Без лечения первичный иммунодефицит приводит к смертности детей от осложнений различных инфекционных болезней.
Симптомы первичного иммунодефицита могут не обнаруживаться у детей, потому что болезнь не имеет уникальных признаков. Это может быть простая, но часто повторяющаяся инфекция, например легких или ЛОР-органов, или проблемы с ЖКТ, воспаления суставов. Часто ни родители, ни врачи не осознают, что все эти проблемы – результат дефекта иммунной системы ребенка. Инфекционные заболевания становятся хроническими, проявляются осложнения, нет реакции на курс антибиотиков. Обычно тяжелые формы иммунодефицита видны сразу после рождения младенца или через некоторое время. Источник:
Доан Тхи Май
Рецидивирующие инфекции у детей – риск иммунодефицита
// Педиатр, 2017, т.8, спецвыпуск, с.109-110
Важно отличать первичный иммунодефицит от СПИДа. Второй – это вирусное, приобретенное заболевание, а первичная форма уже «вживлена» в тело из-за генетических дефектов.
Почему у ребенка появляется вторичный иммунодефицит, и что это такое?
Такое заболевание – это тоже нарушение в работе иммунной системы, оно появляется у детей и взрослых и не является результатом дефектов в генах. Вторичный иммунодефицит может вызывать ряд факторов – внешних и внутренних. Любые внешние неблагоприятные факторы, которые нарушают процесс обмена веществ в организме, могут привести к развитию такой патологии. Самые распространенные из них:
Все эти факторы комплексно воздействуют на организм и все его системы, включая иммунную. А такие, как ионизирующее излучение, избирательно угнетают систему кроветворения. У людей, живущих в условиях загрязненности окружающей среды, снижен иммунитет, они чаще переносят инфекции, увеличиваются риски развития онкологии.
Диагностика ИД
Проводится сбор семейного анамнеза и жалоб ребенка (если он не новорожденный), осмотр, а также ряд лабораторных исследований: молекулярно-генетическое, клинический анализ крови и др.
Важно! Если в семье уже есть ребенок с первичной иммунной недостаточностью, то при вынашивании второго крайне важна пренатальная диагностика.
Признаки и симптомы первичного иммунодефицита обнаруживаются у детей уже в первые недели жизни. Когда врач собирает анамнез, особое внимание он обращает на частую заболеваемость вирусами и бактериальными инфекциями, на наследственность, отягощенную нарушениями работы иммунитета, на врожденные пороки развития.
Нередко такую патологию выявляют намного позже и случайно, когда проводят другие анализы.
Основные методы диагностики как врожденных, так и приобретенных нарушений работы иммунитета:
Лечение заболевания
Первичная форма заболевания предполагает:
Скорректировать иммунодефицит можно, применяя иммунореконструкцию, заместительное лечение, иммуномодуляторы. При первичной форме патологии применяют иммуноглобулины, при вторичной используют иммунотропы, заместительную терапию, иммунизацию.
Крайне важна при первичной патологии изоляция ребенка от всех источников заражения. Когда нет обострений инфекций, ребенок может вести нормальный образ жизни. При первичном иммунодефиците на фоне общей недостаточности антител детей нельзя прививать от:
Проживающим вместе с ребенком можно делать прививки только инактивированными вакцинами.
Противомикробное лечение заключается в приеме антибиотиков широкого спектра. При отсутствии быстрого ответа на терапию препарат меняют. Если же эффект есть, то принимать антибиотик ребенок должен минимум 3-4 недели. Лекарства вводятся внутривенно или парентерально. Одновременно назначают противогрибковые препараты и при показаниях – противовирусные, антипротозойные, антимикобактериальные лекарства. Противомикробная терапия может быть даже пожизненной.
При гриппе на фоне ИД обычно прописывают озельтамивир, ремантадин, занамивир, амантадин, ингибиторы нейраминидазы. Если ребенок заболел «ветрянкой» или герпесом, назначают ацикловир, парагрипп требует приема рибавирина. Перед стоматологическим лечением и операциями ребенок должен пройти курс антибиотиков для профилактики инфекции.
При серьезном вторичном или первичном Т-клеточном ИД нужно профилактировать пневмоцистовую пневмонию, в зависимости от показателей анализов крови. Для этого врачи обычно прописывают триметопримсульфометаксозол.
Важно! Любые лекарства должен назначать только врач, самолечение смертельно опасно для ребенка!
Способы коррекции недостаточности иммунитета:
Иммунореконструкция предполагает пересадку костного мозга или стволовых клеток, которые получают из пуповинной крови. При первичном ИД заместительная терапия – это чаще всего прием аллогенного иммуноглобулина, который в последние годы принято вводить внутривенно.
Лечение детей с первичным ИД с общими дефектами выработки антител
В этом случае проводится заместительная терапия иммуноглобулинами, которые вводятся внутривенно, и антибиотиками. Иммуноглобулины вводятся один раз в три-четыре недели пожизненно. Постоянная терапия антибиотиками нужна для профилактики бактериальных инфекций.
При обострении бактериальной инфекции назначаются антибиотики широкого спектра, вводимые парентерально. При гипер IgM-синдроме и общей вариабельной иммунной недостаточности (ОВИН) нужно постоянно принимать противогрибковые и противовирусные препараты. Они могут назначаться курсами. Это определяется врачом индивидуально. Если у ребенка Х-сцепленный гипер IgM-синдром, то ему показана пересадка костного мозга от HLA-идентичного донора.
Методы лечения вторичного ИД
В основном применяется иммунотропная терапия, которая может быть разных направлений:
Выбор иммунотропной терапии зависит от того, насколько остро выражен воспалительно-инфекционный процесс и какой иммунологический дефект выявлен. Когда симптомы болезни отступают, для профилактики может проводиться вакцинотерапия.
В качестве заместительной терапии применяются иммуноглобулины, вводимые внутривенно. Основное их действующее вещество – специальные антитела, получаемые от доноров. Часто назначаются иммуноглобулины, содержащие только IgG.
Иммунотропное лечение вторичного ИД
С помощью иммуномодуляторов можно повысить эффективность антимикробной терапии. Иммуномодуляторы должны быть частью комплексной терапии совместно с этиотропным лечением инфекции. Схемы и дозировку рассчитывает врач индивидуально.
Во время приема иммуномодуляторов должен проводиться иммунологический мониторинг. Если инфекция находится в острой стадии, иммуномодуляторы применяют с осторожностью. Иначе можно вызывать тяжелый общий воспалительный ответ и септический шок в результате него. Источник:
Г.А. Самсыгина, Г.С. Коваль
Проблемы диагностики и лечения часто болеющих детей на современном этапе
// Педиатрия, 2010, т.89, №2, с.137-145
Способы профилактики
ИД проще предупредить, чем лечить. Важно помнить, что состояние ребенка напрямую зависит от того, насколько правильно планировалась беременность. Если у одного из родителей есть проблемы с иммунитетом, он должен пройти специальные процедуры, чтобы исключить подобную патологию у ребенка.
В первые шесть месяцев жизни рекомендуется только грудное вскармливание, потому что в материнском молоке есть все нужные элементы, способствующие выработке полноценного иммунитета. Если нет лактации, нужны качественные искусственные смеси, но обязательно дополняемые поливитаминами.
Источники:
Рецидивирующие инфекции у детей
Почему маленькие дети так часто болеют, и какие профилактические меры помогут укрепить их иммунитет.
Как часто у детей бывают рецидивирующие инфекции?
Дети рождаются с незрелой иммунной системой, поэтому у младенцев часто бывают инфекционные заболевания, как правило, раз в один-два месяца. Вскоре после рождения иммунная система ребенка начинает развиваться, и со временем частота инфекционных заболеваний уменьшается. Как правило, дети школьного возраста страдают рецидивирующими инфекциями ими не чаще, чем взрослые.
Почему врача могут встревожить рецидивы инфекций у ребенка?
Большинство врачей бьют тревогу, если обычные вирусные инфекции у детей осложняются бактериальными, такими как сепсис или пневмония. Частые или необычные инфекции – тоже повод для беспокойства.
Почему у некоторых детей инфекционные заболевания бывают чаще, чем обычно?
Иногда причины лежат на поверхности. Например, все дело может быть в том, что ребенок ходит в детский сад, где дети прикасаются к общим игрушкам и трогают друг друга, распространяя таким образом инфекцию. Взрослые гораздо меньше контактируют с чужими микробами, поэтому и не заражаются так часто.
Еще одна причина насморка и чихания у маленьких детей – пассивное курение. Поскольку все больше женщин детородного возраста курит, пассивное курение чаще становится причиной респираторных инфекций у детей. Теперь установлена его связь с инфекциями и астмой в детском возрасте.
Могут ли быть причиной рецидивирующих инфекций анатомические особенности?
Распространенная причина рецидивирующих инфекций у детей – особенности строения носовых пазух и евстахиевых труб (каналов, соединяющих среднее ухо с глоткой). Такие инфекции могут передаваться по наследству. У некоторых детей анатомические особенности затрудняют отток отделяемого из евстахиевых труб и носовых пазух, из-за чего бактерии начинают размножаться. Поэтому такие дети более подвержены инфекциям. В большинстве случаев по мере взросления ребенка дренаж улучшается. Детям младшего возраста, слишком часто страдающим ушными инфекциями, может понадобиться лечение антибиотиками или введение специальных трубочек для дренирования среднего уха.
К рецидивирующему синуситу (заложенности носа или появлению выделений из него) и затруднению дыхания могут привести аллергия и астма. Аллергия иногда вызывает длительное раздражение в носу. Из-за него протоки носа и носовых пазух, через которые в норме происходит отток отделяемого, распухают, их просвет закрывается. Бактерии размножаются, приводя к инфекции. В таких случаях нужны лекарства, устраняющие причину болезни, то есть аллергию.
Кашель, сопровождающий вирусную инфекцию, может быть признаком астмы. Таким детям нужны лекарства от астмы в дополнение к другим медикаментам, которые они принимают от инфекции.
Почему у детей бывают тяжелые рецидивирующие инфекции?
Иногда это просто дело случая. Даже здоровые дети могут без видимой причины перенести 2-3 тяжелые инфекции. В таких случаях врач может назначить дополнительные обследования, чтобы убедиться, что у ребенка нет иммунодефицита. Иммунодефицитные состояния – основная причина повторяющихся тяжелых инфекций.
Другими возможными причинами могут быть такие заболевания, как муковисцидоз и СПИД. Муковисцидоз встречается очень редко, а СПИД ребенок в подавляющем большинстве случаев получает от матери.
Как уберечь ребенка от рецидивирующих инфекций?
Все будет хорошо?
У большинства детей, страдающих рецидивирующими инфекциями, нет серьезных проблем со здоровьем, и они вырастут здоровыми людьми. Уже ближе к школьному возрасту они будут болеть гораздо реже. Нужно только заботиться о том, чтобы дети больше спали и правильно питались. Сон и здоровая пища так же важны для борьбы с инфекциями, как и лекарства.
Повторные респираторные инфекции у детей (часто болеющие дети)
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Отечественная педиатрическая наука продолжает оперировать таким термином, как «часто болеющие дети» (ЧБД). В составе этой группы оказываются дети с повторными инфекциями верхних дыхательных путей. Таким образом, состояние, констатация факта повторных инфекций начинают восприниматься как диагноз. Восприятие явления повторных инфекций как диагноза нередко приводит к неоправданной полипрагмазии, отвлечению сил и средств медицинской службы от действительно больных детей. Часто действия врача по отношению к ЧБД оказываются эмпирическими и основываются на бездоказательных рекомендациях. Во избежание подобного роль дифференциальной диагностики и понимание полиэтиологичности заболевания для правильного выбора терапии становятся еще более значимыми.
Острые респираторные инфекции (ОРИ), или простудные заболевания, назофарингит, ринофарингит – инфекции верхних дыхательных путей с первичным и преимущественным поражением носа, сопровождающиеся кашлем, ринореей, конъюнктивитом, болями в горле, лихорадкой, разрешающиеся в подавляющем большинстве случаев самостоятельно в ближайшие 7–10 дней. Некоторые признаки могут сохраняться до 3 нед. Инфекции уха, горла, носа, а также бронхолегочные инфекции составляют основной перечень заболеваний в детском возрасте [1, 2]. Дети первых 5 лет жизни, посещающие дошкольные учреждения, переносят до 8 эпизодов ОРИ в год при полностью сохранном иммунитете [3, 4]. Сезонное увеличение числа случаев респираторных инфекций, которые в России, Европе и США традиционно трактуются как простудные (common cold), известно даже в тропиках в сезон дождей, и там точно также обсуждается та же самая проблема врачебной тактики [5].
Существует более 250 инфекционных агентов, вирусов и бактерий, вызывающих респираторные заболевания. Самый частый возбудитель ОРИ (до 80%) – риновирус, вариант пикорнавируса, насчитывающий более 90 серотипов. Часто выявляются коронавирусы, вирусы гриппа (10–15%), парагриппа, аденовирусы (5–7%), респираторный синцитиальный вирус, метапневмовирус и другие. Нередко у обследованных выявляется два и более вируса. Спектр инфекционных агентов достаточно стабилен, и частотное соотношение возбудителей ОРИ, обнаруженных независимыми исследователями в разных странах Европы и даже Африки, весьма сильно совпадает [6].
Чем теснее контактируют люди (детские сады, школа, общежития, перенаселенная квартира, транспорт мегаполисов), тем быстрее распространяется инфекция. Получена положительная корреляционная связь между длительностью пути на работу и респираторной заболеваемостью. ОРИ традиционно называются и трактуются как простудные заболевания. Но холод сам по себе не вызывает респираторных заболеваний. Их причина – вирусы или бактерии. Подъем заболеваемости в холодное влажное время года объясняют длительным нахождением аэрозольных капель во влажном воздухе, местными изменениями респираторного тракта в ответ на холод, сниженным иммунным ответом, длительным нахождением детей в помещении и началом занятий в школе.
Но в практических условиях педиатр всегда стремится исключить сложные заболевания, протекающие под маской рецидивирующих респираторных инфекций. Такие дети нередко направляются на консультативные приемы с подозрением на иммунодефицит (ИД).
Следует различать физиологическую и патологическую склонность к инфекции. В физиологических состояниях ребенок, даже переносящий повторные респираторные инфекции, растет и развивается нормально, будучи выведен из привычного коллектива на дачу, каникулы, перестает болеть. В семейном анамнезе нет родственного брака. Перенесенная инфекция оставляет иммунитет и защищает от реинфекции этим же вирусом. Живые вакцины не приводят к поствакцинальным инфекциям. Нет системных инфекций, нет персистенции инфекции и атипичных возбудителей, выздоровление – без дефекта. Вилочковая железа, миндалины, аденоиды, лимфатические узлы в период инфекции увеличиваются в размерах [7].
Для ИД [8] характерно необычное течение инфекций (высокая частота, затяжное и осложненное течение, оппортунистическая инфекция и т.д.). И при таком развитии заболевания часто рассматривается применение иммуномодулирующих препаратов. Но возможно необычное течение инфекций без признаков ИД. Это типично для следующих синдромов:
• нарушение кровообращения, в т.ч. на уровне микроциркуляции, врожденные и приобретенные пороки сердца и магистральных сосудов, тяжелые хронические анемии, сахарный диабет;
• обструкции полых органов: стенозы мочеточника или уретры, бронхиальная астма, бронхоэктазы, муковисцидоз, синдром нарушенного мерцания ресничек, нарушение проходимости евстахиевой трубы (анатомические вариации, аденоидные вегетации);
• дефекты питания и состояния с потерей белка, стрессы, мальнутриция любого генеза, нефротический синдром, белковотеряющая энтеропатия, экзема, ожоги, переломы больших костей;
• инородные тела: шунты вентрикулярные при гидроцефалии, внутрисосудистые стенты, катетеры, искусственные клапаны сердца, водители ритма, аспирированные или забытые при операциях инородные тела;
• необычная манифестация собственно микробного фактора: рост необычной флоры после ятрогенной элиминации привычных возбудителей, хроническая инфекция устойчивыми микроорганизмами, постоянная реинфекция (употребление зараженных продуктов или воды, пребывание в зараженной атмосфере птичников, зооферм, лабораторий и т.д., постоянный контакт с человеком или животным – носителями инфекции; контаминированные кондиционеры, ингаляторы и медицинский инструментарий).
Отправными пунктами для диагностики и дифференциальной диагностики первичных ИД являются рецидивирующие инфекции, их высокая частота, краткие или вообще отсутствующие бессимптомные промежутки, резистентность инфекции к терапии, необычное течение болезни или необычная инфекция, труднообъяснимые или тяжелые осложнения [9, 10]. Разработаны 10 настораживающих признаков первичных иммунодефицитных состояний:
1. Наличие у родственников больного первичных ИД, ранних смертей от тяжелых инфекций или одного из нижеперечисленных состояний.
2. Отставание грудного ребенка в весе и росте.
3. Персистирующая молочница или грибковое поражение кожи в возрасте старше 1 года.
4. Заболевания отитом не менее 6–8 раз за год.
5. Несколько подтвержденных серьезных синуситов (не менее 4–6 раз в течение года).
6. Более двух подтвержденных пневмоний.
7. Повторные глубокие абсцессы кожи и внутренних органов.
8. Потребность в длительной терапии антибиотиками для купирования инфекции (до 2 мес. или дольше).
9. Потребность во внутривенной антибиотикотерапии для купирования инфекции.
10. Не менее двух таких инфекций, как менингит, остеомиелит, сепсис.
Если у пациента обнаружено 2 и более только что перечисленных признаков, то диагноз ИД вероятен.
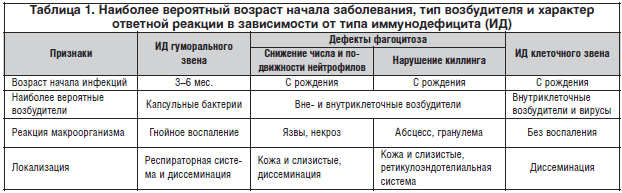
Для правильной диагностики имеют значение возраст дебюта патологии, общий статус пациента, преимущественная топическая локализация инфекции, ее вид и ответная реакция макроорганизма [11]. При первичных ИД, кроме В-иммунодефицита, нередко отмечается задержка умственного развития. Тип инфекции достаточно характерен для определенного вида ИД. Пневмококки и стрептококки излюбленно поражают людей с В-клеточным (антительным) дефицитом. Тяжелые вирусные, грибковые и другие оппортунистические инфекции указывают на Т-клеточный дефицит. Возвратные инфекции грамотрицательной флорой и стафилококками нередко сопровождают детей с нарушенным фагоцитозом, а Neisseria – с дефицитом компонентов комплемента (табл. 1). Типирование возбудителя должно строиться непосредственно на его выявлении, т.к. иммунологические методы в условиях невозможности антительного ответа или клеточной реакции могут дать ложноотрицательные результаты. Лабораторная диагностика ИД проводится по этапам (табл. 2):
1 этап – поликлинический и общие лечебные учреждения;
2 – специализированные учреждения.
Среди детей дошкольного возраста, наблюдаемых как часто болеющие респираторными вирусными инфекциями, до 30–40% составляют дети с бронхиальной астмой легкого течения [12]. Подтверждением этого является то, что большая группа т.н. ЧБД в поликлиническом звене нередко имеет в индивидуальных картах такие сопутствующие состояния, как «респираторный аллергоз», «обструктивный бронхит» и т.д. Поэтому при исключении случаев физиологической реакции на инфекцию следует помнить о возможной бронхиальной астме. Повторные ОРИ, наслаиваясь на аллергически воспаленную слизистую, способны у генетически предрасположенных людей вызывать гиперреактивность бронхов. Признаками респираторной аллергии могут быть только хронический ринит и кашель как эквивалент астмы. Респираторную аллергию следует исключать при наличии следующих признаков:
1. респираторные симптомы не сопровождаются лихорадкой. Отделяемое из носа водянистого характера;
2. регистрируются признаки атопии;
3. в индивидуальном анамнезе есть указания на атопический дерматит или непереносимость отдельных видов пищи;
4. в семейном анамнезе есть случаи атопического дерматита, экземы, аллергического ринита или астмы;
5. ухудшение состояния развивается сезонно или после экспозиции с определенным веществом, растением или животным;
6. антибиотики малоэффективны;
7. облегчение приносят антигистаминные препараты и бронходилататоры.
В случае исключения органических причин повторных респираторных инфекций встает проблема выбора оптимальной терапии, сочетающей эффективность и безопасность при общей доступности.
При определении тактики ведения детей с повторными случаями ОРИ необходимо исключить наличие аденоидитов, тонзиллофарингитов, требующих соответствующего лечения. После этого дискутируется возможность назначения иммуномодулирующей терапии. Наиболее часто применяемые в детской практике иммуномодуляторы относятся к препаратам синтетического и бактериального происхождения. Единственным лекарственным препаратом природного происхождения является натрия нуклеинат.
Этот биопрепарат имеет хорошую доказательную базу. Так, in vitro натрия нуклеинат продемонстрировал возможность снижения продукции провоспалительных цитокинов мононуклеарами периферической крови человека (IL-6, ИФ-γ), а также оказался эффективным ингибитором LPS-индуцированного сепсиса в экспериментах in vivo [17]. Кроме того, дальнейшее изучение натрия нуклеината выявило его способность увеличивать противовоспалительную функциональную активность моноцитов/макрофагов за счет регулирования синтеза активных форм кислорода [18]. В эксперименте также показана способность натрия нуклеината снижать активность процесса хронического воспаления, улучшая гистологические показатели его течения [15].
Длительность применения препарата в клинике с возможностью анализа его эффективности при различных состояниях позволила сделать оптимистические выводы [13, 14]. Назначение натрия нуклеината часто болеющим пациентам приводит к повышению качества жизни, общей активности, работоспособности, снижению утомляемости с положительным иммуномодулирующим и иммунопрофилактическим эффектом. Препарат назначался по 2 капсулы 2 раза/сут. и не вызывал побочных действий [16].
Помимо иммуномодулирующей терапии требуются режимные мероприятия, связанные с закаливанием, регуляцией контактов.
Таким образом, проблема часто и длительно болеющих детей является весьма актуальной. Требуется исключение состояний, имитирующих банальные респираторные инфекции и требующих специализированной помощи. Тактика врача определяется преморбидным состоянием ребенка, наличием аденоидита, тонзиллофарингита. В лечении наряду с общеукрепляющими процедурами обсуждается применение иммуномодулирующих препаратов как синтетического, так и природного происхождения.
Литература
1. Доклад о состоянии здоровья населения Москвы в 2008 г. / Правительство Москвы. Департамент здравоохранения. Управление Роспотребнадзора по городу Москве. М., 2009. 174 с.
2. Доклад о состоянии здоровья населения Москвы в 2009 г. / Правительство Москвы. Департамент здравоохранения. Управление Роспотребнадзора по городу Москве. М., 2010. 172 с.
3. Альбицкий В.Ю., Баранов А.А. Часто болеющие дети. Клинико-социальные аспекты. Пути оздоровления. Саратов, 1986. 165 c.
4. Rieger C., Hardt H. (Hrsg.) Padiatrische Pneumologie. Springer, Berlin, 1999. 1157 s.
5. Perera B. Bacterial immunostimulants in recurrent pediatric respiratory infections // Sri Lanka Journal of Child Health, 2011. Vol. 40. P. 43–44.
6. Siegenthaler W. (Hrsg.) Differentialdiagnose innnerer Krankheiten. 17. neubearbeitete Auflage. Stuttgart: Geirg Thieme Verlag, 1993.
7. Slatter M., Gennery A. Clinical Immunology Review Series: An approach to the patient with recurrent infections in childhood // Clin. Experim. Immunol. 2008. Vol. 152. P. 389–396.
8. Кондратенко И.В., Бологов А.А. Первичные иммунодефициты. М.: Медпрактика-М, 2005. 232 с.
9. Champi C., Primary immunodeficiency disorders in children: prompt diagnosis can lead to lifesaving treatment // J. Pediatr. Health Care. 2002. Vol. 16. P. 16–21.
10. Rich R., Fleisher Th., Shearer W. et al. (Ed.) Clinical immunology. Principles and practice. London: Mosby, 2003. Vol. 1, 2.
11. Beers M., Berkow R. (Eds.) The Merck Manual of Diagnosis and Therapy. 17-th Edition, 1999. 2833 p.
12. Зиновьева Н.В., Давыдова Н.В., Щербина А.Ю. и др. Часто болеющие дети: чем они больны на самом деле // Трудный пациент. 2007. № 2. С. 40–43.
13. Земсков А.М., Передерий В.Г., Земсков В.М. и др. Иммунокорригирующие нуклеиновые препараты и их клиническое применение. Киев: Здоровье, 1994. 232 с.
14. Катеруша Е.И. Клинико-иммунологические особенности и эффективность иммунотерапии у больных рецидивирующими формами зоба: автореферат дисс… к.м.н. Саратов, 2012. 28 с.
15. Шевченко А.Н., Коваленко Л.И. Клеточно-тканевая динамика воспаления на фоне введения натрия нуклеината // Український морфологічний альманах. 2011. Т. 9, № 4. С. 149–151.
16. Семидоцкая Ж.Д., Чернякова И.А., Бездетко Т.В. и др. Опыт применения нуклеината в лечении длительно и часто болеющих пациентов // Новости медицины и фармации. 2007. № 16.
17. Jukic T., Abidov M., Ihan A. A. tetrahydrophthalazine derivative «sodium nucleinate» exerts a potent suppressive effect upon LPS-stimulated mononuclear cells in vitro and in vivo // Coll Antropol. 2011 Dec; 35 (4):1219–23.
18. Jukic T., Ihan A., Jukic D. Tetrahydrophthalazine derivative «sodium nucleinate» exert its anti-inflammatory effects through inhibition of oxidative burst in human monocytes // Coll Antropol. 2012 Jun; 36 (2): 409–12.


